«Старение» плаценты Текст научной статьи по специальности «Клиническая медицина»
рэс
і-=>■
АКТУАЛЬНЫЕ ПРОБЛЕМЫ ЗДРАВООХРАНЕНИЯ
Э.К. Айламазян’, «СТАРЕНИЕ» ПЛАЦЕНТЫ
Е.А. Лапина2, И.М. Кветной1
‘Научно-исследовательский институт
акушерства и гинекологии
им. Д.О. Огта РАМН, Санкт-Петербург;
2Институт биорегуляции и геронтологии СЗО РАМН,
Санкг- Петербург
■ Представлен анализ современных данных о структурно-функциональных изменениях в плаценте в конце беременности. Согласно традиционным представлениям, сложившимся еще
в начале XX века, инволютивные процессы, возникающие в плаценте в течение относительно короткого периода нормальной беременности отражают ее «старение» как органа. Подробно рассмотрены структурнофункциональные изменения последа, традиционно описываемые как признаки «старения» плаценты: отложения фибриноиза, образование кальцификатов, инфарктов плаценты и другие признаки. С другой стороны, представлены данные, свидетельствующие об активном росте и функциональной активности плаценты в конце беременности: образование терминальных ворсин и синцитиокапиллярных мембран, обеспечивающих максимальную площадь обмена между материнской и плодовой кровью, рост и регенерация ворсин.
Эти признаки служат доказательством отсутствия в нормально развивающейся плаценте инволютивных процессов, а те из них, которые расцениваются как проявление «старения», на самом деле являются следствием патологических изменений, возникающих в плаценте при патологии беременности. Патологические состояния беременности, для которых характерно проявление признаков «старения» плаценты, описываются в данном обзоре. Анализируется участие биологически активных молекул в механизмах контроля плацентарного роста, дифференцировки и инволюции.
Патологические состояния беременности, для которых характерно проявление признаков «старения» плаценты, описываются в данном обзоре. Анализируется участие биологически активных молекул в механизмах контроля плацентарного роста, дифференцировки и инволюции.
■ Ключевые слова: плацента, старение, трофобласт, терминальные ворсины, фибриноид.
В настоящее время предметом дискуссий остается вопрос: подвергается ли плацента старению или нет? Существуют две основные концепции, описывающие функциональные и структурные изменения в плаценте в конце беременности.
Согласно первой наиболее консервативной концепции, в процессе относительно короткого периода нормальной беременности происходит «старение» плаценты [30, 36, 37]. Признаки «старения» плаценты появляются в разное время, чаще в начале третьего триместра беременности. Сторонники данной гипотезы считают, что по мере созревания плода и становления его собственных систем жизнеобеспечения, снижается потребность в трофических, гормональных, газообменных, иммунных и выделительных функциях плаценты. В связи с этим происходит физиологическая редукция соответствующих структур, которая начинается после 32 недели, но особенно выражена при сроке беременности свыше 42 недель и проявляется рядом атрофических, склеротических и дистрофических процессов, сходных с изменениями, возникающими при физиологическом старении органов [2]. Эта точка зрения основана на результатах сопоставления клинических, структурных и функциональных данных и в ней не учитываются различия между временными изменениями этого органа и процессами «старения».
Согласно другой точки зрения, к концу беременности в плаценте накапливаются различные структурные повреждения, которые можно оценить как патологические ее изменения. Функциональная активность плаценты к концу беременности снижается, однако это не является показателем процесса старения. Некоторые исследователи выделяют присутствие в «стареющей» плаценте признаков дополнительного адаптивного созревания [29].
Некоторые исследователи выделяют присутствие в «стареющей» плаценте признаков дополнительного адаптивного созревания [29].
Плацентарный рост и функциональная активность плаценты в конце беременности
В течение девятого месяца беременности практически завершается формирование плаценты путем образования котиледонов и разделительных септ. Доминирующим типом ворсин становятся терминальные ворсины, которые составляют весомую часть ворсинчатого дерева на восьмом и девятом месяцах и частично сохраняются в течение последнего месяца гестации и составляют 45—50% всех ворсин, а в доношенной плаценте 20%. Это многочисленные «листья дерева», отходящие главным обра
зом от промежуточных дифференцированных ветвей и стволовых ворсин II и III порядка. В доношенной плаценте они покрыты преимущественно синцитиотрофобластом, но более 20% их поверхности занимают двухслойные участки с подлежащим цитотрофобластом.
Терминальные специализированные ворсинки активно формируются в последние недели беременности. Все капилляры терминальных ворсинок превращаются в широкие синусоиды, которые концентрируются под истонченными, безъядерными участками синцитиотрофобласта и образуют истинные синцитиокапиллярные мембраны или плацентарный барьер. Помимо изолированных ворсин встречаются гроздевидные их скопления, соединенные синцитиокапил-лярными почками-мостиками [4].
Процессы созревания ворсинчатого дерева и функциональная дифференцировка трофоблас-та приводят к появлению преобладающих ворсинчатых форм, оптимально адаптированных к механизмам материнско-плодового обмена. Вышеперечисленные морфологические изменения значительно увеличивают площадь обмена между материнской и плодовой кровью [12, 15], что обеспечивает более активный обмен веществ [27].
Долгое время считалось, что плацентарный рост и синтез ДНК прекращаются к 36 недели беременности, и что любое увеличение размера плаценты происходит скорее за счет увеличения размера клеток, чем увеличения их числа [39]. Это суждение легко опровергается с помощью простых гистологических исследований, которые показали, что в центре плацентарных долей имеются области для устойчивого роста, представленные незрелыми промежуточными ворсинками. Более того, концентрация ДНК значительно выше во втором и третьем триместрах по сравнению с первым [18] и общее содержание плацентарной ДНК продолжает равномерно увеличиваться вплоть до 42 недели беременности [31]. Ауторадиографические и цитометрические исследования подтверждают продолжающийся синтез ДНК в плаценте [19, 22], ас помощью морфометрических методов показан устойчивый рост ворсинок, продолжающееся расширение ворсинчатой поверхности и прогрессивное разветвление ворсинчатого дерева [12, 23].
В течение последних недель беременности плацентарный рост замедляется, но не останавливается. Однако при неблагоприятных условиях, например, при тяжелой степени анемии у матери, плацента может продолжать увеличиваться в размерах. Как правило, увеличение плацентарного роста на поздних сроках беременности
сопровождается процессами старения, которые проявляются не только в плаценте, но и в других органах матери. Большее сходство плацента обнаруживает с печенью, так как именно печень формирует долго живущие постмитотические клетки и обладает сходным потенциалом для клеточной пролиферации и возможного роста [16].
Плацента обладает широким спектром компенсаторных реакций на всех уровнях структурной организации. Практически эти реакции направлены на активизацию многообразных плацентарных функций и главным образом на увеличение диффузной способности органа. Так, «старение» и дегенерация ворсин в нормально созревающей плаценте человека компенсируется посредством регенерации ворсинчатого дерева. Важно подчеркнуть, что в процессе регенерации эпителия ворсин участвуют только недифференцированные и промежуточные формы цитотро-фобласта. Процессы регенерации эпителия тесно связаны с ростом новых терминальных ворсин и регулируются путем изменения градиента парциального давления кислорода [11]. Утрата способности к регенерации ворсин может вызвать хронические нарушения у плода, получающего питательные вещества за счет недостаточного количества терминальных ворсин [13].
Так, «старение» и дегенерация ворсин в нормально созревающей плаценте человека компенсируется посредством регенерации ворсинчатого дерева. Важно подчеркнуть, что в процессе регенерации эпителия ворсин участвуют только недифференцированные и промежуточные формы цитотро-фобласта. Процессы регенерации эпителия тесно связаны с ростом новых терминальных ворсин и регулируются путем изменения градиента парциального давления кислорода [11]. Утрата способности к регенерации ворсин может вызвать хронические нарушения у плода, получающего питательные вещества за счет недостаточного количества терминальных ворсин [13].
Следует отметить, что активность ферментов, вовлеченных в синтез эстрогенов в ворсинчатом хорионе, на протяжении всей беременности не изменяется [26].
Таким образом, плацента к 10-му месяцу гестации представлена полностью сформированным в функциональном отношении органом; общая поверхность всех ворсин составляет огромную величину — 12,5 м2 [11]. Наличие тонкого и протяженного плацентарного барьера в терминальных и особенно специализированных ворсинах, а также значительный объем межвор-синчатого кровотока объясняют удивительный факт интенсивной прибавки массы плода при незначительном приросте массы плаценты в течение последнего месяца.
Функциональная морфология «старения» плаценты
Ряд структурных преобразований, которые происходят в плаценте, начиная с третьего триместра, и особенно в конце беременности, получили название признаков «старения» плаценты. К ним относят отставание массы плаценты от роста плода, уменьшение функциональной активной поверхности хориона, а также уменьшение емкости межворсинчатого пространства [1].
К проявлениям «старения» плаценты обычно относят и накопление фибриноида. Фибриноид является наиболее частой микроскопической находкой при исследовании плаценты.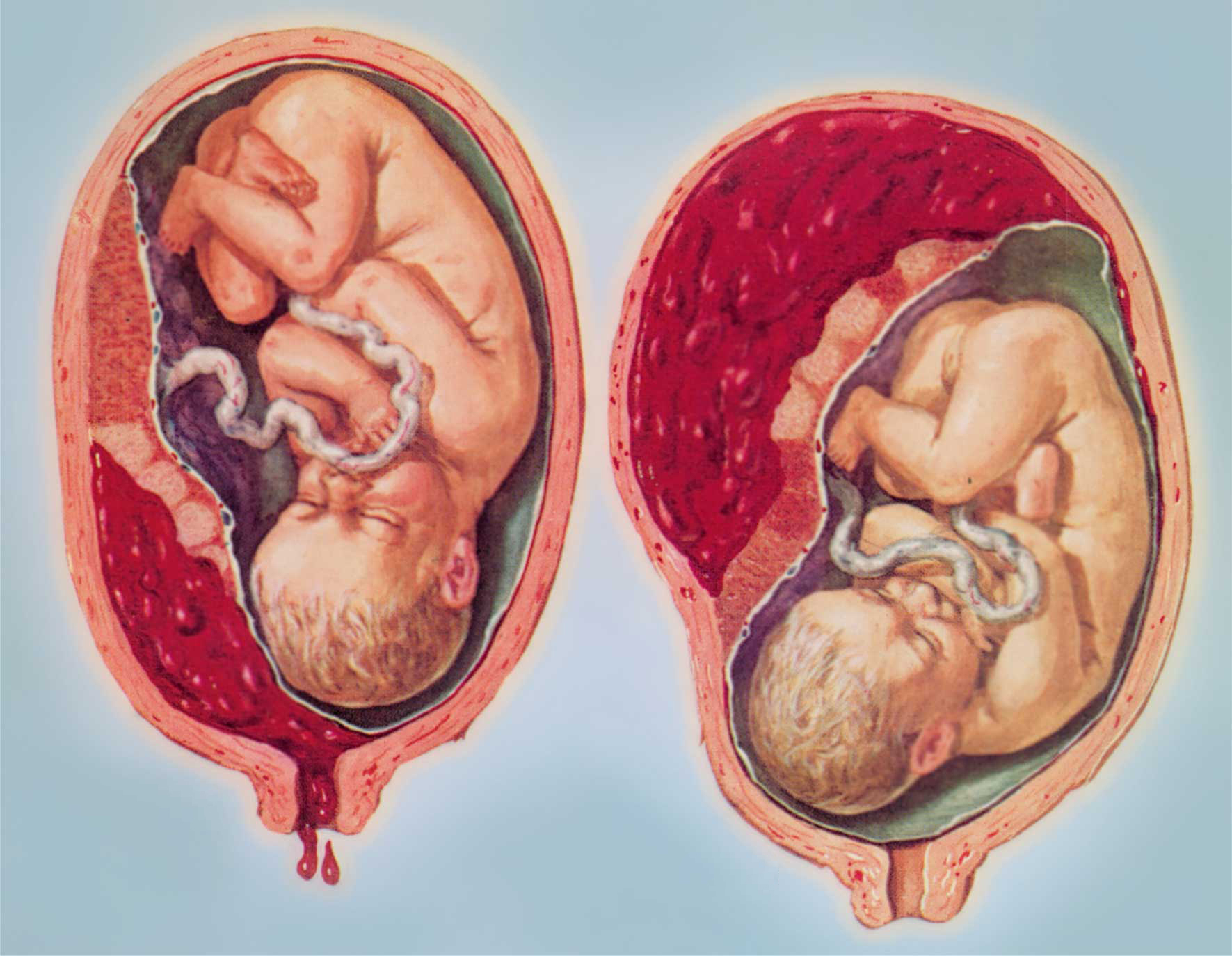 Взгляды разных авторов на его значение существенно отличаются. Одни обращают внимание на возможность его выявления в «нормальных» плацентах, другие связывают его со «старением» последа, а третьи объясняют его появление самыми разнообразными патологическими процессами.
Взгляды разных авторов на его значение существенно отличаются. Одни обращают внимание на возможность его выявления в «нормальных» плацентах, другие связывают его со «старением» последа, а третьи объясняют его появление самыми разнообразными патологическими процессами.
Уже в начале XX века предпринимались попытки изучить химический состав фибриноида и доказать его неоднородность. В связи с этим на протяжении многих лет использовали два термина: «фибрин» и «фибриноид». Впервые фибрин и фибриноид были выделены Гроссером в 1925—1927 годах из аморфных отложений плаценты. Фибрин рассматривался как преципитат фибриногена крови в тканевых жидкостях, а фибриноид — как сходная с фибрином субстанция гетерогенного происхождения [1].
Результаты многочисленных биохимических и иммуногистохимических исследований последних лет изменили ранее принятую терминологию. Термин «фибрин» использоваться перестал. Фибриноид стал подразделяться на два варианта: фибриноид фибринового типа (fibrin type fibrinoid) и фибриноид матричного типа (matrix tipe fibrinoid). Первый из них рассматривается как продукт свертываемости крови материнского и плодового происхождения. Фибриноид матричного типа содержит единичные окруженные матриксом тро-фобластические клетки и характеризуется позитивной иммуногистохимической реакцией с антителами к онкофетальному фибронектину, коллагену IV типа и ламинину. Фибриноид фибринового типа по-видимому участвует в построении межворсинчатого пространства, а также защищает поврежденный трофобласт, выступая в роли транспортного и иммунного барьера. Фибриноид матричного типа является секреторным продуктом вневорсинчатого трофобласта и, возможно, выполняет инвазивную функцию [17].
Места отложения фибриноидов обоих типов несколько варьируются. В слое Лангганса, начальных сегментах стволовых ворсин и глубоких слоях базальной пластинки (слой Нитабуха) и клеточных островках наиболее часто выявляются оба типа фибриноида одновременно. Тонкие полоски, окружающие ворсины, в том числе стволовые, обычно представлены фибриноидом фибринового типа. Для фибриноида матричного типа наиболее характерны отложения в клеточных островках и в глубине клеточных колонок.
Тонкие полоски, окружающие ворсины, в том числе стволовые, обычно представлены фибриноидом фибринового типа. Для фибриноида матричного типа наиболее характерны отложения в клеточных островках и в глубине клеточных колонок.
Фибриноиду приписывается множество функций. В первые месяцы развития плода это веще-
ство играет цементирующую роль для объединения различных клеток матери и плода, а также ему присуща роль адгезива для прикрепления к маточной стенке. В более поздний период, в основном до 20 недель беременности, развитые слои фибриноидного вещества образуют эффективную преграду против дальнейшего внедрения трофобласта. Кроме того, фибриноид принимает участие в регуляции вневорсинчатого кровообращения, в формировании плаценты при ее созревании и в материнско-фетальных транспортных процессах [1, 3, 7, 9].
Большинство исследователей рассматривают фибриноид как субстанцию, имеющую иммунологическое значение. Фибриноид на поверхности ворсин в местах соприкосновения материнской крови со структурами плаценты можно рассматривать как своеобразную антигенную ловушку, препятствующую массивному проникновению антигенов, в том числе вирусов к плоду. Возможно, что сиаловая кислота, входящая в состав фибриноида, способна маскировать фетальные гены и предотвратить их распознавание материнскими клетками, в том числе сенсибилизированными лимфоцитами. С другой стороны, фибриноид маскирует антигенные свойства зародыша [1].
К инволютивно-дистрофическим изменениям плаценты относятся также инфаркты, возникающие в результате тромбоза плодных сосудов. Термином «инфаркты» принято обозначать (особенно в клинической практике) все узелки на поверхности и в паренхиме плаценты величиной от простого зерна до куриного яйца. С точки зрения микроскопического строения и механизма возникновения между этими узелками имеются существенные различия, позволяющие разделить их в зависимости от происхождения на четыре группы: истинные инфаркты плаценты, межворсинчатые тромбы и гематомы, отложения фибрина и кистозную дегенерацию плацентарных перегородок [1].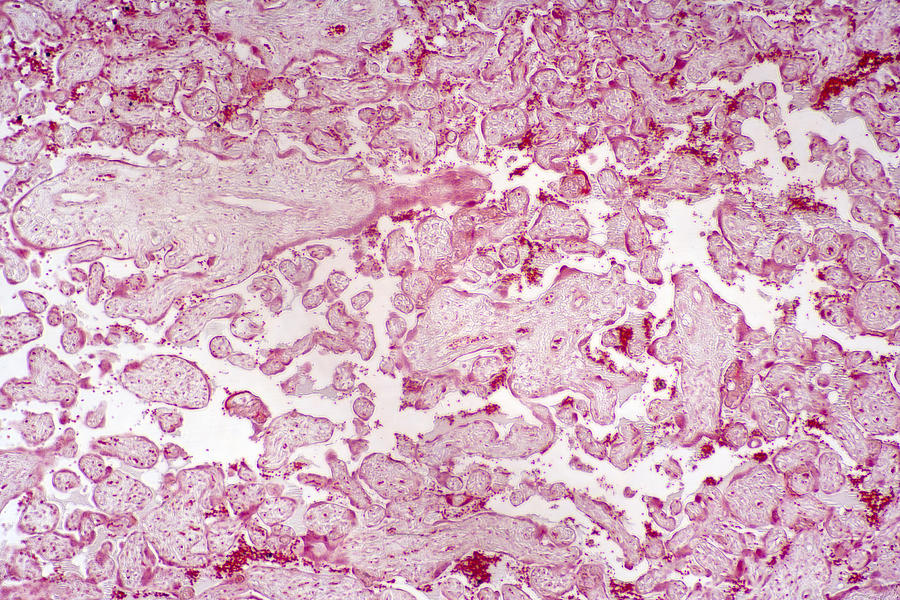 Другие авторы считают, что описание инфарктов носит формально морфологический характер [9].
Другие авторы считают, что описание инфарктов носит формально морфологический характер [9].
Кальцификация является общим признаком, свойственным плацентам человека. Особенности кальцификации плаценты человека сходны с процессами физиологической и патологической кальцификации в других тканях [35].
Обнаружение кальцификатов в плаценте является предметом дискуссий: одни авторы считают их предметом дегенерации децидуальной ткани, другие рассматривают их как кальциевое депо для плода, третьи как признак переношенной беременности. Существует мнение, что отложения солей кальция в плаценте отражает ост-
рые нарушения в обмене кальцием и витаминами [5]. По мнению Говорка (1970) кальцифика-ты не имеют какого-либо клинического значения. Согласно традиционному представлению, на поздних сроках беременности, позже 32-й недели в хориальном эпителии откладывается известь в виде кристаллов, глыбок и бесформенных масс. Позже обызвествлению подвергаются плацентарные перегородки, хориальная пластинка, массы фибриноида, тромбы.
Таким образом, небольшие очаги или единичные мелкие кальцификаты постоянно выявляются в плаценте при нормальной беременности; они являются ультразвуковым признаком зрелости плаценты. Однако при переношенной беременности, антенатальной гибели плода и многих неясных причинах обнаруживается патологическое обызвествление как проявление минеральной дистрофии [4].
Появление признаков старения в плаценте, как считают сторонники теории «старения» плаценты, несомненно, является результатом глубоких биологических изменений в трофобласте. Последний в конце беременности становится все больше морфологически и функционально малоактивной полупроницаемой оболочкой с постоянно уменьшающейся поверхностью [1]. Происходит сужение межворсинчатого пространства, уменьшение диаметра ворсин хориона, уплотнение стромы, истончение хориального эпителия, исчезновение клеток Кащенко—Гофбауэра и клеток Ланханса [2].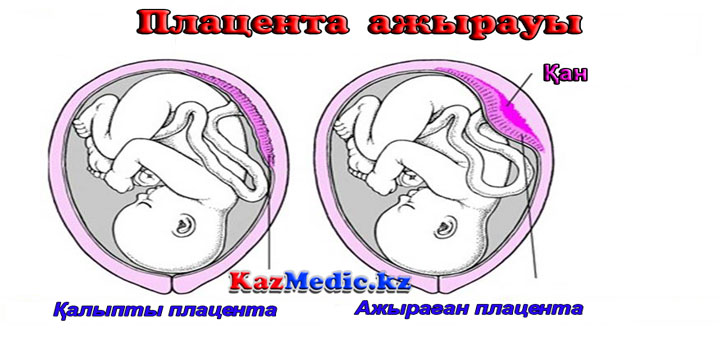
По поводу последнего критерия «старения» в литературе существуют противоречивые данные. Так, одни авторы считают, что характерным признаком физиологического «старения» плаценты является сохранение пролиферативного потенциала трофобласта, наличие отдельных камбиальных клеток Ланханса и незрелых промежуточных ворсин, которые определяются не только при доношенной (38—40 недель), но и при пролонгированной (40—42 недель) беременности [2]. По данным других авторов, сохранение слоя Ланханса до конца беременности при различных нарушениях в течении беременности является важным диагностическим признаком [1]. С помощью иммуногистохимических методов показано, что в третьем триместре беременности наблюдается увеличение апоптозного индекса в плаценте, прежде всего в трофобласте по сравнению с первым триместром [25, 33].
Атрофические изменения ворсин хориона имеют безусловное физиологическое значение, поскольку сопровождаются выраженным истончением плацентарного барьера (в среднем до 3-4 мкм) и тем самым в значительной мере снижают
напряженность обменных процессов между матерью и плодом. Следствием этого является редукция фетоплацентарного и маточно-плацентар-ного кровообращения, особенно выраженная в краевых отделах плаценты. Происходит спазм и облитерация стволовых артерий, раскрытие ар-терио-венозных анастомозов, уменьшение числа функционирующих капилляров в терминальных ворсинах хориона. Интенсивность обеспечения кровью плацентарного ложа заметно ослабевает на 10-м месяце беременности [4].
По мнению противников теории «старения» плаценты, все вышеперечисленные структурные преобразования могут лишь условно относиться к признакам «старения» плаценты. А.В. Цинзер-линг (1993) считает, что, по крайней мере, часть изменений плаценты из числа традиционно рассматриваемых как нормальные на самом деле являются проявлением патологических процессов, в частности, инфекционных.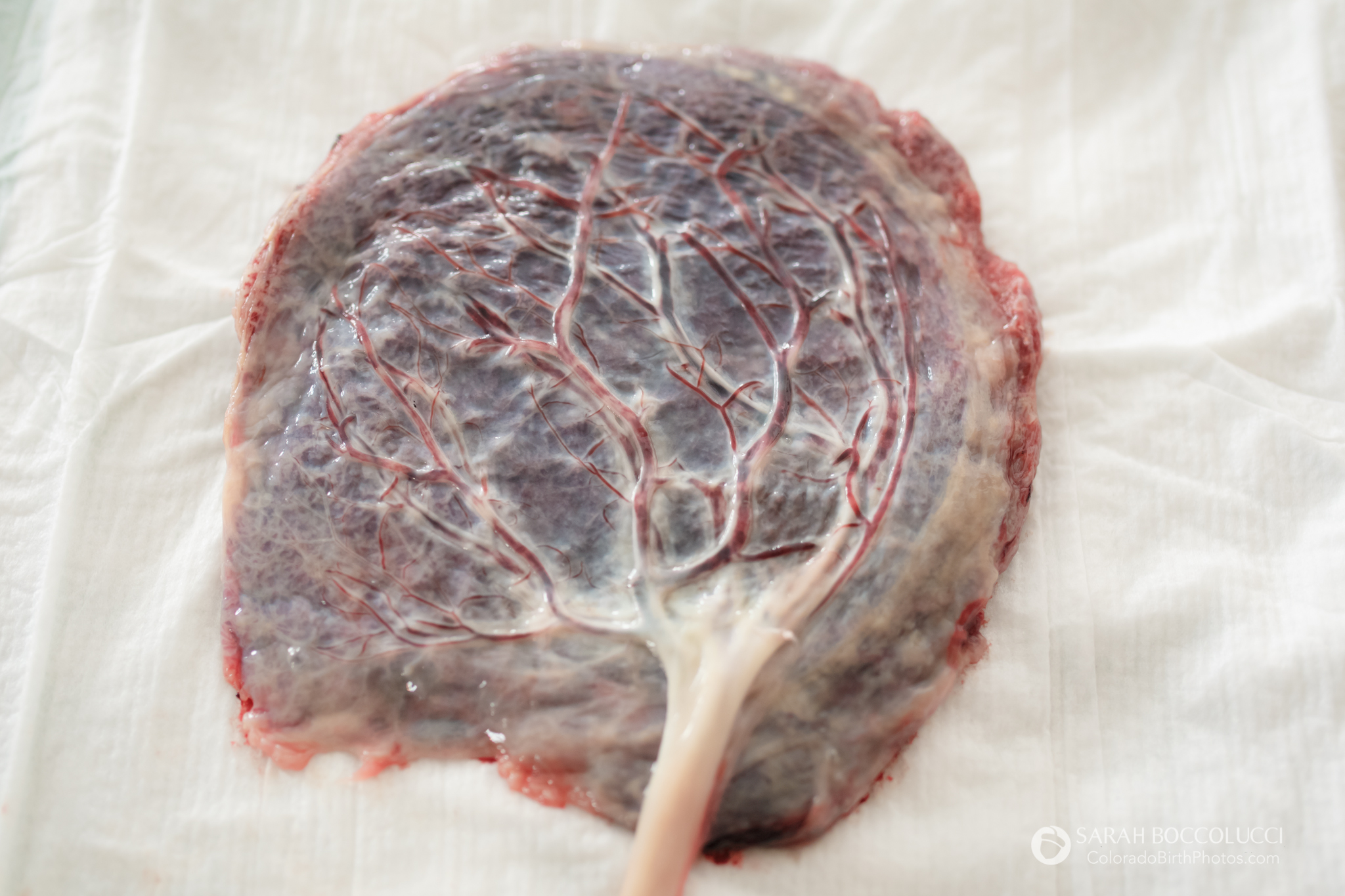 Так, присутствие фибриноида в интервиллезном пространстве свидетельствует также о нарушении свертываемости плацентарной крови, поскольку в норме кровь обладает сниженной свертываемостью.
Так, присутствие фибриноида в интервиллезном пространстве свидетельствует также о нарушении свертываемости плацентарной крови, поскольку в норме кровь обладает сниженной свертываемостью.
По мнению А.П. Милованова, плацентарный фибриноид типичных локализаций является неотъемлемой структурной особенностью нормальной плаценты и формируется на протяжении всего ее развития. Это образование следует считать физиологической структурой, отражающей закономерную эволюцию плаценты и взаимодействие двух элементов (материнской крови и вневорсинчатого цитотрофобласта).
Морфологические изменения при «старении» плаценты не оказывают влияния на плод и на кровоток в пупочной и маточной артериях, не вызывают высокого риска осложнения беременности, а также инфарктов плаценты и ее структурных аномалий [24]. Таким образом, на наш взгляд инволюционные процессы не следует относить к патологии, они возникают при достижении необходимого уровня структурнофункциональной зрелости плаценты. Такая «физиологическая инволюция» не оказывает неблагоприятного влияния на состояние плода.
Клиническая патология и функциональная морфология плаценты в конце беременности
По мнению ряда авторов, преждевременное созревание плаценты по своей морфогенетической сущности обозначает ускорение созревания ворсин хориона, которые ранее обычного срока достигают состояния, характерного для доношенной беременности.
Преждевременное созревание ворсин относится к разряду неспецифических процессов, которые могут возникать при гестозах, невынашивании беременности и любых других обстоятельствах, сопровождающихся гипоксией [10]. Преждевременная дифференцировка терминальных ворсин, как правило, сопровождается избыточной пролиферацией ядер хориального синцития зрелых промежуточных и терминальных ворсин хориона, что ведет к появлению множественных синцитиальных узелков. При этом плацента выглядит старше своего гестационно-го возраста и, например, в 35—36 недель может соответствовать строению доношенной плаценты. Происходит увеличение числа типичных терминальных ворсин, которые в норме появляются с 32-й недели и их количество достигает максимума к 36-й неделе. Как правило, большинство из них содержит несколько узких капилляров в центре стромы; они не формируют истинных синцитиокапиллярных мембран, т. е. не соответствуют специализированному типу терминальных ворсин, которые образуются в течение последнего месяца беременности [4].
При этом плацента выглядит старше своего гестационно-го возраста и, например, в 35—36 недель может соответствовать строению доношенной плаценты. Происходит увеличение числа типичных терминальных ворсин, которые в норме появляются с 32-й недели и их количество достигает максимума к 36-й неделе. Как правило, большинство из них содержит несколько узких капилляров в центре стромы; они не формируют истинных синцитиокапиллярных мембран, т. е. не соответствуют специализированному типу терминальных ворсин, которые образуются в течение последнего месяца беременности [4].
В качестве компенсаторных изменений в плацентах при гестозе происходит повышенная вас-куляризация предсуществующих терминальных ворсин, что ведет к гиперплазии зрелого ворсинчатого дерева и тем самым повышает функциональную активность плаценты, обеспечивающую адекватную компенсацию имеющейся недостаточности маточно-плацентарного кровообращения [6].
Преждевременное созревание плаценты нередко расценивается в качестве компенсаторно-приспособительной реакции. Компенсаторно-приспособительные реакции нацелены на сохранение или даже на усиление функциональной активности плаценты, что в полной или частичной мере способствуют восстановлению нарушенного гомеостаза плода. Компенсаторно-приспособительные реакции плаценты имеют динамический характер, в связи с чем при устранении или ослаблении этиологического фактора могут подвергаться инволюционным изменениям.
Преждевременное «старение» плаценты связано с повышенным риском беременности, задержкой внутриутробного роста и низким весом плода. Созревание плаценты, соответствующее сроку беременности, является хорошим прогностическим признаком для развития плода [34].
Если бы плацента подвергалась процессам старения, то маловероятно, что она сохраняла бы способность нормально функционировать и поддерживать рост зародыша даже после 40-й недели созревания, что наблюдается при синдроме «перезрелого» младенца [16].
В настоящее время не вызывает сомнений тот факт, что пренатальная смертность при переношенной беременности не связана с какими-либо функциональными изменениями плаценты. Изучение плацент при переношенной беременности не выявило каких-либо крупных изменений плаценты, таких как инфаркты, кальцификация или массивные межворсинчатые отложения фибрина. Наиболее частое гистологическое отклонение, наблюдаемое при переношенной беременности, — слабая фетальная перфузия в плацентарных ворсинках. При этом сосуды плода в ворсинчатом хорионе не имеют каких-либо изменений. Слабая перфузия плаценты наблюдается при маловодии, так как кровь зародыша в данном случае поступает в плаценту менее активно [20].
Следует отметить, что патофизиология переношенной беременности до конца не изучена. Однако четко установлено, что любые патологические проявления у плода при переношенной беременности не связаны с плацентарной незрелостью или «старением» плаценты [16].
Сигнальные молекулы: контроль созревания и инволюции плаценты
Сигнальные молекулярные механизмы созревания плаценты до конца не изучены. Экспериментальные исследования показали, что вся программа генетического развития плаценты, включая инвазию, дифференцировку, рост и старение плодовой части плаценты, может модулироваться с помощью различных факторов: кислорода, белков внутриклеточного матрикса, цитокинов, факторов роста, простагландинов, лейкотриенов и гормонов.
Слияние клеток цитотрофобласта и функциональная дифференцировка ворсинчатого тро-фобласта специфично регулируется глюкокор-тикоидами и хорионическим гонадотропином (ХГЧ). Эти гормоны также играют физиологическую роль в дифференцировке трофобласта. ХГЧ может быть очень важен на ранних сроках беременности, когда его продукция максимальна, в то время как эстриол, продуцируемый плацентой, и кортизол, секретируемый почками плода, могут быть вовлечены в поздние стадии созревания и «старения» трофобласта [26]. Согласно гипотезе, предложенной Сгошег и соавт., продукция стероидных гормонов может влиять на морфологические и функциональные изменения трофобласта в период гестации, в частности, эстрадиол стимулирует образование синцития и секрецию ХГЧ. Эстрадиол также необходим для созревания трофобласта [14].
Согласно гипотезе, предложенной Сгошег и соавт., продукция стероидных гормонов может влиять на морфологические и функциональные изменения трофобласта в период гестации, в частности, эстрадиол стимулирует образование синцития и секрецию ХГЧ. Эстрадиол также необходим для созревания трофобласта [14].
В процессы дифференцировки, созревания и «старения» плаценты вовлечено множество генов. Ген PL74/gdfl5/MIC-l и семейство цито-кинов TGF-(3 контролируют апоптоз и диффе-ренцировку трофобласта. Развитие трофобласта определяется также генами PL48 серин-треонин протеин киназы, РВК-1, туникамицин-контро-лирующим геном, катепсин D-подобным геном (DAP-1) и генами, продукты которых вовлечены в процесс возникновения гипоксии (HRF-1,2,6,8 и HIF-l-a, HIF-1-P и hepas-1). Слияние клеток цитотрофобласта индуцирует ген синцитии и ERF-3. Эндоглин, P1GF, TGF-P 3, IGF-II, IGFBP-1 и плацентарная IGFBP протеаза участвуют в регуляции пролиферации цитотрофо-бласта и его инвазии. Гомеозисные гены DLX4, НВ24, MSX2 и МОХ2 также играют роль в развитии эпителиально-мезенхимных отношений в плаценте. Транскрипционные факторы, такие как TEF-5, Hand 1, НЕВ, HASH-2 и два продукта гена EST играют регуляторную роль в развитии плаценты [28, 32].
Циклин Е, активирующий циклинзависимую киназу-2, обычно экспрессируется в опухолевых тканях и отсутствует в нормальных тканях; он регулирует клеточную пролиферацию, диффе-ренцировку и старение. Повышенная экспрессия циклина Е может быть связана с процессами старения и неэффективной адаптацией плаценты [13].
Важная роль в процессе развития и инволюции ворсинчатого древа принадлежит различным факторам васкуляризации (эндотелиальные факторы, факторы капиллярного роста и др.). Утверждение о том, что гипоксия может стимулировать ангиогенез [38] и, следовательно, иметь значительную роль в плацентарном развитии, подтверждает концепцию об ускоренном плацентарном созревании, наблюдаемом в некоторых случаях преэклампсии.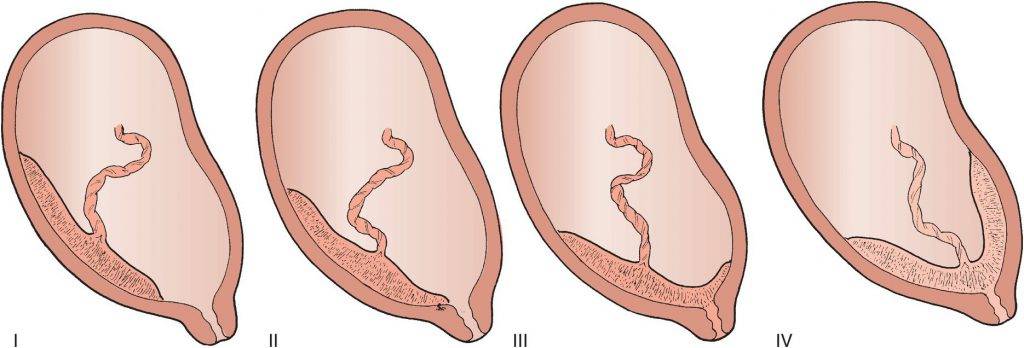 В плацентах с изменениями кровотока наблюдается раннее старение экстраклеточного матрикса (с преобладанием коллагена I типа в периваскулярном пространстве). В стареющей плаценте с помощью иммунногистохимических методов идентифицируются HLA-DR+ клетки, что говорит о нормальных взаимоотношениях между плодовыми антигенами и популяции Т-клеток даже на поздних сроках беременности [21].
В плацентах с изменениями кровотока наблюдается раннее старение экстраклеточного матрикса (с преобладанием коллагена I типа в периваскулярном пространстве). В стареющей плаценте с помощью иммунногистохимических методов идентифицируются HLA-DR+ клетки, что говорит о нормальных взаимоотношениях между плодовыми антигенами и популяции Т-клеток даже на поздних сроках беременности [21].
В заключение следует отметить, что механизмы, детерминирующие продолжительность жизни трофобласта плаценты, еще неизвестны, не смотря на то что одновременно эти же механизмы участвуют в определении срока родов. Современные достижения генетики развития позволяют согласиться с мнением исследовате-
лей, считавших еще в 20-х годах XX века, что продолжительность существования трофобласта генетически детерминирована.
Еще в середине XX столетия известный классик отечественной плацентологии А.И. Брусиловский писал: «…мы постепенно приближаемся к прочтению плаценты как визитной карточки плода…». Тщательный анализ современных молекулярно-биологических данных формирования и развития плаценты человека позволяет нам считать несостоятельной теорию «старения» плаценты и утверждать, что описанные морфофункциональные изменения плаценты в процессе беременности являются не следствием инволюции, а закономерными компенсаторными реакциями, направленными на обеспечение нормального роста и развития плода.
Литература
1. Говорка Э. Плацента человека. — Варшава: Польское государственное медицинское издательство, 1970. -470 с.
2. Калашникова Е.П. Клинико-морфологические аспекты плацентарной недостаточности // Арх. пат. — 1988. —
B. 5. — С. 99-105.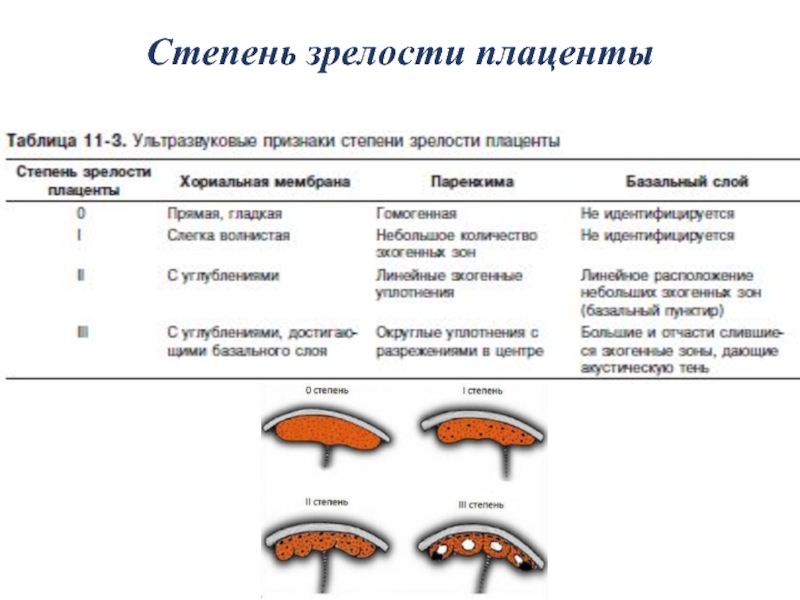
3. Калашникова Е.П. Патологическая диагностика недостаточности плаценты при различных формах патологии матери // Арх. пат. — 1986. — № 9. —
C. 14-20.
4. Милованов А.П. Патология системы мать-плацента-плод. — М.: Медицина, 1999. — 448 с.
Б. Михайлова Н.П. Гистоэнзиматические особенности плаценты в норме и при некоторой акушерской патологии. — Горький: Горьковский медицинский институт, 1977. — 73 с.
6. Савельева Г.М., Федорова М.В., Клименко П.А., Сичинава Л.Г. Плацентарная недостаточность. — М.: Медицина, 1991. — 276 с.
7. Субботин М.Я., Донских Н.В., Брусиловский А.И., Новиков В.Д. Плацента человека // Сборник научных статей: «Гистофизиология и гистопатология внезародышевых органов человека и млекопитающих». -Новосибирск, 1971. — С. 3~62.
8. Цинзерлинг А.В. Современные инфекции.
Патологическая анатомия и вопросы патогенеза. — СПб.: Сотис, 1993. — 363 с.
9. Цинзерлинг В.А., Мельникова В.Ф. Перинатальные инфекции. Вопросы патогенеза, морфологической диагностики и клинико-морфологических сопоставлений: Практическое руководство. — СПб.:
Элби СПб, 2002.
10. Becker V. Patologie der Austerfung der Placenta. In . Die Placenta des Menchen. Becker V., ShieblerTh.H., Kubli F. (eds.). — Stuttgart, 1981. — S. 266-281.
11. Benirschke K, Kaufmann P. // Patology of the Human Placenta. — 3rd ed. — New York: Springer-Verlag, 1990. -720 p.
12. Boyd P.A. Quantitative studies of the normal human placenta from 10 weeks of gestation to term // Early Hum. Devel. — 1984. — Vol. 9. — P. 297-307.
Boyd P.A. Quantitative studies of the normal human placenta from 10 weeks of gestation to term // Early Hum. Devel. — 1984. — Vol. 9. — P. 297-307.
13. Bukovsky A, Cekanova M, Caudle MR et al. Variability of placental expression of cyclin E low molecular weight variants // Biol Reprod. — 2002. — Vol. 67, N. 2. —
P. 568 74.
14. Cronier L, Guibourdenche J, Niger C, Malassine A. Oestradiol stimulates morphological and functional differentiation of human villous cytotrophoblast //
Placenta. — 1999. — Vol. 20, N. 8. — P. 669-676.
15. Fenley M.R., Burton G.J. Villous composition and membrane thickness in the human placenta at term:
a stereological study using unbiased eximators and optimal fixation techniques // Placenta. — 1991. — Vol. 12. -P. 131-142.
16. Fox H. Aging of the placenta // Arch Dis Child Fetal Neanatal Ed. — 1997. — Vol. 77. — P. 171-175.
17. Frank H-G., Malekzadeh F., Kertschanska S. et al. Immunohistochemistry of two different types of placental fibrinoid //Acta Anat. — 1994. — Vol. 150. — P. 55-68.
18. Fukuda M, Okuyama T, Furuya H. Growth and function of the placenta — with special reference to various enzymes involved in the biosynthesis of steroids in the human placenta // Nippon Sanka Fujinka Gakkai Zasshi. — 1986. -Vol.38, N. 3. — P. 411-416.
19. Geier G., Schuhman R., Kraus H. Regional unterschliedliche Zellproliferation innerhalb der Placentome reifer menschlicher Placenten: autoradiographische Untersuchungen // Arch Gynacol. — 1975. — Vol. 218. —
— 1975. — Vol. 218. —
P. 31-37.
20. Gill R. W., Warren P.S., Garrett IV. J., Kossoff G., Stewart A. Umbilical vein blood flow. Chervenack F.A., Isaacson G.C., Campbell S. eds. // Ultrasound in obstetrics and ginecology. Boston: Little, Brown. — 1993. — Vol. 3. — P. 587-595.
21. Giordano-Lanza G, Soscia A, Montagnani S. Morpho-functional aspects of human placental vessels // Ital J Anat Embryol. — 1995. — Vol. 100, N. 1. — P. 309-316.
22. Iverson I.E., Farsund T. Flow cytometry in the assessment of human placental growth. Acta Obstet Scand. — 1985. -Vol. 64. — P. 605-607.
23. Jackson M.R., Mayhew T.M., Boyd P.A. A quantitative description of the elaboration and maturation of villy from 10 weeks of gestation to term // Placenta. — 1992. — Vol. 13. -P. 357-370.
24. Kara SA, Toppare MF, Avsar F, Caydere M. Placental aging, fetal prognosis and fetomaternal Doppler indices // Eur J Obstet Gynecol Reprod Biol. — 1999. — Vol. 82, N. 1. -P. 47-52.
25. Kudo T, Izutsu T, Sato T. Telomerase activity and apoptosis as indicators of ageing in placenta with and without intrauterine growth retardation. // Placenta. — 2000. -Vol. 21, N5-6.-P. 493-500.
26. Malassine A, Cronier L. Hormones and human trophoblast differentiation: a review // Endocrine. — 2002. — Vol. 19, N1,- P. 3-11.
27. Mayhew T.M., Jackson M.R., Boyd P.A. Changes in oxygen diffusive conductances of human placentae during gestation (10-41 weeks) are commensurate with the gain in fetal
feight // Placenta. — 1993. — Vol. 14. — P. 51-61.
— 1993. — Vol. 14. — P. 51-61.
28. Morrish D. W., Dakour J., Li H. Life and death in the placenta: new peptides and genes regulating human syncyniotrophoblast and exnravillous cytotrophoblast lineage formation and renewal // Curr Protein Pept Sci. — 2001. — Vol. 2, N 3. — P. 245-259.
29. Parmley T. Placental senescence // Adv Exp Med Biol. —
1984. — Vol. 176. — P. 127-32.
30. Rosso P. Placenta as an ageing organ // Curr Concept Nutr. — 1976. — Vol. 4. — P. 23-41.
31. Sands J., Dobbing J. Continuing growth and development of third trimester human placenta. — 1985. — Vol. 6. — P. 13—22.
32. Simpson H., Robson S.C., Bulmer J.N. et al. Transforming growth factor beta expression in human placental bed during early pregnancy // Placenta. — 2002. — Vol. 23, N 1. —
P. 44-58.
33. Smith S.C., Baker P.N., Symonds E.M. Placental apoptosis in normal human pregnancy. // Am J. Obstet Gynecol. -1997. — Vol. 177, N 1. — P. 57-65.
34. Valenzuela B.A., Mendez G.A. Premature aging of the placenta. Ultrasonic diagnosis // Ginecol Obstet Mex. -1995.-Vol. 63.-P. 287-292.
35. Varma VA, Kim KM. Placental calcification: ultrastructural and X-ray microanalytic studies j I Scan Electron Microsc. —
1985. — Vol. 4. — P. 1567-72.
36. Vincient R.A., Huang P.C., Parmley T.H. Proliferative capacity of cell cultures derived from the human placenta // In vitro. — 1976.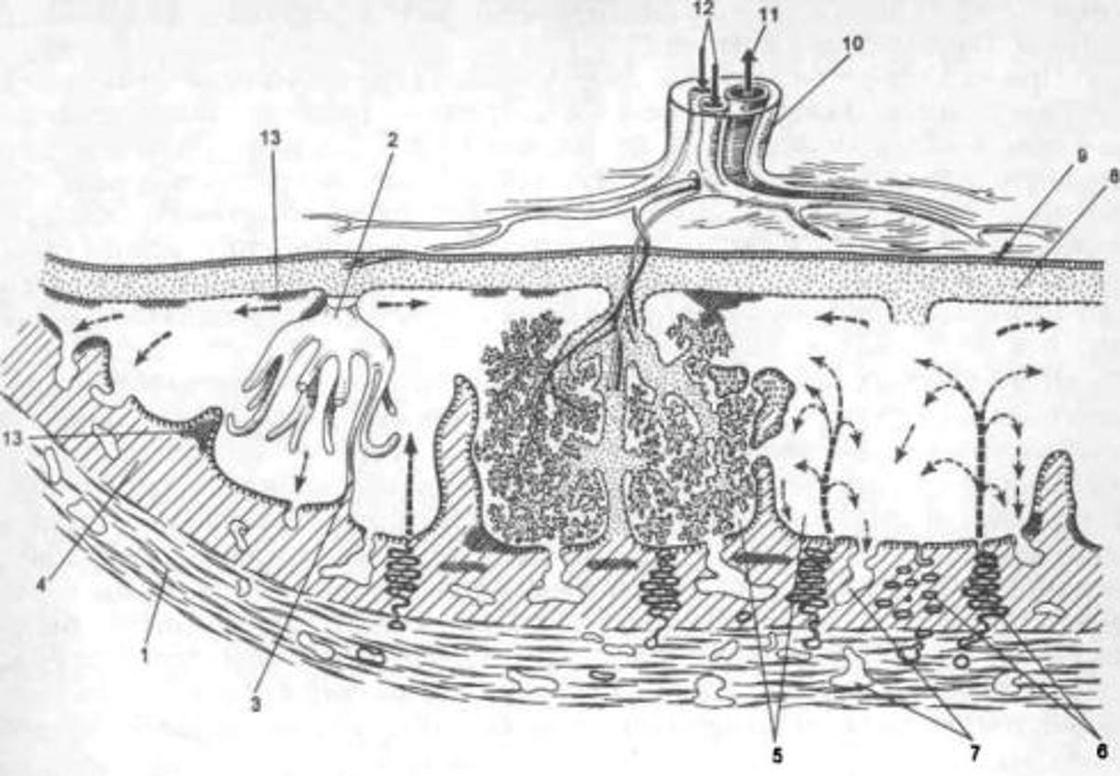 — Vol. 32. — P. 649-653.
— Vol. 32. — P. 649-653.
37. Vorherr H. Placental insufficiency in relation to posterm pregnancy and fetal postmaturity: evaluation of fetoplacental function: management of the postterm gravida // Am J.
Obstet Gynecol. — 1975. — Vol. 123. — P. 67-103.
38. Wheeler T., Elcock C.L., Anthony F.W. Angiogenesis and placental environement // Placenta. — 1995. — Vol. 16. -P. 289-296.
39. Winick M, Coscia A., Noble A. Cellular growth in human placenta. 1. Normal cellular growth // Pediatrics. — 1967. -Vol. 39.-P. 248-251.
«AGING» OF PLACENTA
Ailamazyan E.K., Lapina E.A., Kvetnoy I.M.
■ The summary: As the nature of any intrinsic biologic aging process or even of its existence independent of disease is unknown, it is impossible to state whether or not the placenta gets old. There are two main conceptions to describe the morphological and physiological changes of placenta at term. It is widely believed that during the relatively short duration of normal pregnancy the placenta progressively ages and is, at term, on the verge of decline into morphological and physiological senescence. Several placental functions decrease near term, but it is impossible to attribute these to aging. In fact, some of them may represent adaptive additional maturation or pathological processes. The genetic differentiation/invasion/maturation programs of placental cells could be modulated by their environment: oxygen, extracellular matrix, and soluble factors (cytokines, growth factors, and hormones).
■ Key words: placenta, aging, trophoblast, terminal villi, fibrinoid.
Ранее старение плаценты Риск рождения крупного плода — Гинекология
Отвечает Коноваленко Наталия Владимировнагинеколог
Здравствуйте!
Для оценки течения беременности, функции плаценты и состояния плода производится регулярное клиническое наблюдение; динамическое ультразвуковое обследование в 1, П и Ш триместрах; доплерометрия; исследование системы гемостаза, определение содержания эстриола, прогестерона, хорионического гонадотропина и ᾱ-фетопротеина в сыворотке крови; определение содержания окситоциназы, общей и плацентарной щелочной фосфатазы в сыворотке крови, исследование экскреции эстриола с мочой, кольпоцитологическое исследование.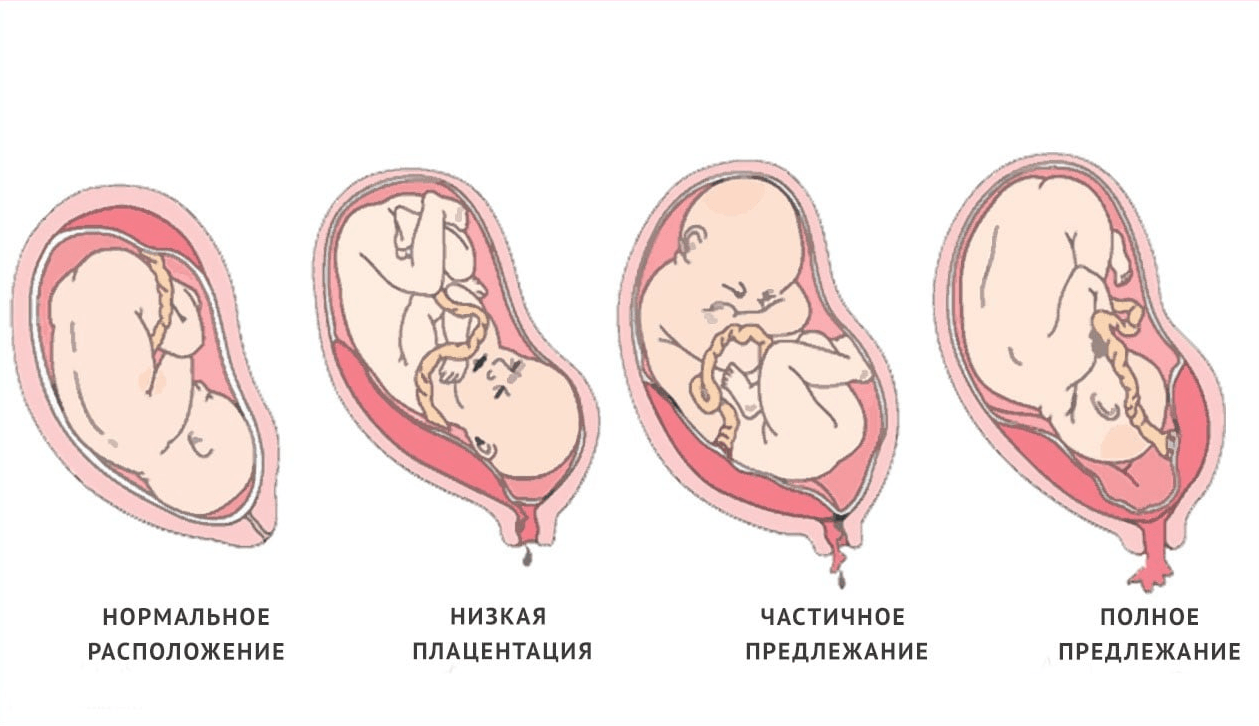 Плацента человека – уникальный орган, который выполняет чрезвычайно разнообразные функции: от синтеза и депонирования необходимых для нормального роста плода веществ, иммунологической защиты фетального аллотрансплантата в процессе развития беременности, участия в материнско-плодовом кровообращении до индуцирующего и регулирующего влияния на родовой акт.
Роль плаценты как органа, обеспечивающего формирование и рост плода, чрезвычайно велика как при физиологической беременности, так и при осложнённом её течении. С целью предупреждения или ослабления возможных неблагоприятных влияний на плод важно своевременно и правильно оценивать состояние плаценты.
Строение и функции плаценты непостоянны. Они меняются с увеличением срока беременности, что связано с возрастающими потребностями развивающегося плода и в значительной мере обусловлено состоянием маточно-плацентарного кровообращения. В настоящее время не вызывает сомнений тот факт, что полноценное развитие плода во многом определяется адекватной маточно-плацентарной гемодинамикой, которая, в свою очередь, зависит от анатомо-морфологических особенностей плаценты.
В процессе развития плаценты следует различать стадии дифференциации, роста, зрелости и старения, направленные на удовлетворение потребностей развивающегося плода.
С внедрением в клиническую практику УЗИ появилась возможность получения информации о расположении, размерах и структуре плаценты.
Хорошо известно, что эхоструктура плаценты меняется с увеличением срока беременности. Этот процесс связан с инволютивно-дистрофическими процессами, начинающимися в основном в конце П триместра и носящими название «старение плаценты».
В повседневной практике врачам УЗИ приходится оценивать ультразвуковую картину плаценты весьма субъективно.
УЗ плацентография позволяет определить соответствие степени зрелости плаценты сроку беременности согласно критериям общепринятой классификации. Постепенное дозревание плаценты с прогрессированием беременности – процесс физиолоический.
Плацента человека – уникальный орган, который выполняет чрезвычайно разнообразные функции: от синтеза и депонирования необходимых для нормального роста плода веществ, иммунологической защиты фетального аллотрансплантата в процессе развития беременности, участия в материнско-плодовом кровообращении до индуцирующего и регулирующего влияния на родовой акт.
Роль плаценты как органа, обеспечивающего формирование и рост плода, чрезвычайно велика как при физиологической беременности, так и при осложнённом её течении. С целью предупреждения или ослабления возможных неблагоприятных влияний на плод важно своевременно и правильно оценивать состояние плаценты.
Строение и функции плаценты непостоянны. Они меняются с увеличением срока беременности, что связано с возрастающими потребностями развивающегося плода и в значительной мере обусловлено состоянием маточно-плацентарного кровообращения. В настоящее время не вызывает сомнений тот факт, что полноценное развитие плода во многом определяется адекватной маточно-плацентарной гемодинамикой, которая, в свою очередь, зависит от анатомо-морфологических особенностей плаценты.
В процессе развития плаценты следует различать стадии дифференциации, роста, зрелости и старения, направленные на удовлетворение потребностей развивающегося плода.
С внедрением в клиническую практику УЗИ появилась возможность получения информации о расположении, размерах и структуре плаценты.
Хорошо известно, что эхоструктура плаценты меняется с увеличением срока беременности. Этот процесс связан с инволютивно-дистрофическими процессами, начинающимися в основном в конце П триместра и носящими название «старение плаценты».
В повседневной практике врачам УЗИ приходится оценивать ультразвуковую картину плаценты весьма субъективно.
УЗ плацентография позволяет определить соответствие степени зрелости плаценты сроку беременности согласно критериям общепринятой классификации. Постепенное дозревание плаценты с прогрессированием беременности – процесс физиолоический.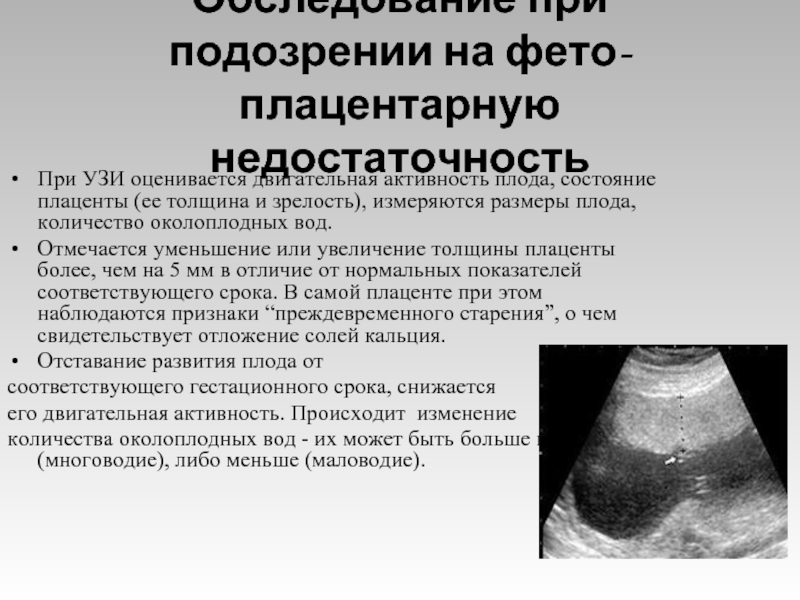 Обычно он начинается с периферических отделом плаценты распространяется к центру и морфологически характеризуется пролиферацией синцития трофобласта, появлением участков некроза (омертвения) ворсин, фибриноидными и истинными инфарктами. В конце беременности часто визуализируются эхопозитивные включения небольших размеров. Морфологически они соответствуют мелким участкам кальцинатов, которые возникают в связи с процессом старения плаценты.
По данным эхографии, в развитии нормальной плаценты различают четыре стадии. При неосложнённом течении І степень зрелости плаценты наблюдается на 30-32 неделе беременности, ІІ – на 34-36 недель, ІІІ – на 37-38 неделе. Время появления определённой степени зрелости плаценты не всегда постоянно. Граница переходного периода с 0 степени зрелости до І отвечает 27-30 неделям беременности, з І до ІІ – 32-34 неделям, з ІІ до ІІІ – 35-37 неделям.
Несоответствие степени зрелости плаценты сроку беременности сопровождается высоким риском развития перинатальных осложнений. Наиболее часто при расстройствах состояния плодово-маточно-плацентарного кровотока отмечается опережение степени зрелости плаценты относительно срока беременности.
Клиническими проявлениями вторичной плацентарной недостаточности являются гипоксия плода, синдром задержки внутриутробного развития плода (СЗВРП), ослойка плаценты, внутриутробная смерть плода.
При хронической плацентарной недостаточности изменяется толщина плаценты и её структура. В плаценте появляются патологические включения.
Допплерометрические исследования позволяют выяснить нарушения циркуляции в системе мать-плацента-плод в группе беременных высокого риска, характеризуют состояние сосудистой резистентности в маточных артериях, артерии пуповины и средней мозговой артерии плода.
Однако если по УЗИ Ваш срок беременности соответствует 33-34 неделям, а плацента соответствует 35-36 неделям, то ничего страшного в этом нет, если состояние Вашего будущего ребёнка не вызывает никаких опасений.
Обычно он начинается с периферических отделом плаценты распространяется к центру и морфологически характеризуется пролиферацией синцития трофобласта, появлением участков некроза (омертвения) ворсин, фибриноидными и истинными инфарктами. В конце беременности часто визуализируются эхопозитивные включения небольших размеров. Морфологически они соответствуют мелким участкам кальцинатов, которые возникают в связи с процессом старения плаценты.
По данным эхографии, в развитии нормальной плаценты различают четыре стадии. При неосложнённом течении І степень зрелости плаценты наблюдается на 30-32 неделе беременности, ІІ – на 34-36 недель, ІІІ – на 37-38 неделе. Время появления определённой степени зрелости плаценты не всегда постоянно. Граница переходного периода с 0 степени зрелости до І отвечает 27-30 неделям беременности, з І до ІІ – 32-34 неделям, з ІІ до ІІІ – 35-37 неделям.
Несоответствие степени зрелости плаценты сроку беременности сопровождается высоким риском развития перинатальных осложнений. Наиболее часто при расстройствах состояния плодово-маточно-плацентарного кровотока отмечается опережение степени зрелости плаценты относительно срока беременности.
Клиническими проявлениями вторичной плацентарной недостаточности являются гипоксия плода, синдром задержки внутриутробного развития плода (СЗВРП), ослойка плаценты, внутриутробная смерть плода.
При хронической плацентарной недостаточности изменяется толщина плаценты и её структура. В плаценте появляются патологические включения.
Допплерометрические исследования позволяют выяснить нарушения циркуляции в системе мать-плацента-плод в группе беременных высокого риска, характеризуют состояние сосудистой резистентности в маточных артериях, артерии пуповины и средней мозговой артерии плода.
Однако если по УЗИ Ваш срок беременности соответствует 33-34 неделям, а плацента соответствует 35-36 неделям, то ничего страшного в этом нет, если состояние Вашего будущего ребёнка не вызывает никаких опасений. Ибо П степень зрелости плаценты наблюдается в сроке беременности 34-36 недель. Граница переходного периода с 1 до П степени зрелости – 32-34 недели. Всё у Вас так, как должно быть.
Всего Вам доброго!
Ибо П степень зрелости плаценты наблюдается в сроке беременности 34-36 недель. Граница переходного периода с 1 до П степени зрелости – 32-34 недели. Всё у Вас так, как должно быть.
Всего Вам доброго!
Преждевременное старение плаценты при беременности: причины, последствия, консультация врача
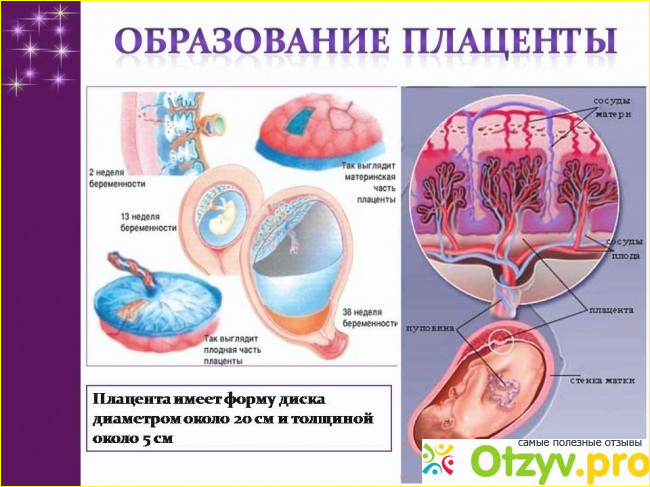
Плацента это эмбриональный орган, основными функциями которого являются защита от инфекций, выработка необходимых гормонов, доставка к плоду кислорода и питательных веществ. Любые нарушения связанные с плацентой будут негативно сказываться на состоянии будущей матери и ребенка, в большей или меньшей степени. Сформировавшаяся плацента представляет собой орган дискообразной формы, диаметр которой составляет примерно 200 мм, а вес около 0,5-0,6 кг. При этом толщина стенок плаценты в это время достигает примерно 30-40 мм. Как и любой другой орган человеческого организма, плацента подвержена старению и это является нормальным процессом, однако в некоторых случаях может произойти преждевременное ее старение.
Причины и последствия преждевременного старения плаценты
Раннее старение детского места может быть обусловлено индивидуальными особенностями организма будущей матери, а также по причине патологического влияния на ее плаценту. К этим патологиям относятся:
- тяжелый токсикоз (гестоз), который появляется во второй половине срока беременности;
- влияние на организм токсических веществ;
- резус-конфликт;
- травмы матки;
- курение;
- хронические болезни почек, сердца, печени, сосудов;
- многоплодная беременность;
- неправильная диета;
- аборты;
- эндокринные заболевания;
- предыдущие тяжелые роды;
- предлежание плаценты или ее частичная отслойка;
- злоупотребление алкоголем;
- развитие инфекций в полости матки.
Результатом вышеуказанных патологий может стать развитие у будущей матери фетоплацентарной недостаточности, которая впоследствии негативно скажется на кровоснабжении ребенка.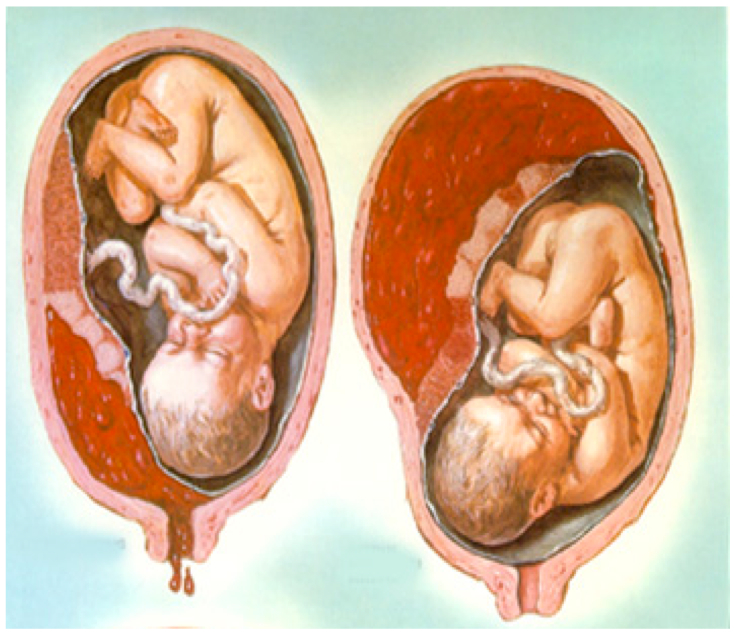 Незначительное нарушение, как правило, компенсируется за счет особенностей организма беременной женщины, однако при более серьезной патологии кровообращения происходит недостаточное снабжение малыша кислородом и питательными веществами. При таких обстоятельствах плод начинает недобирать в весе, происходит нарушение развития всех его органов, последствием чего может стать тяжелые роды, недоразвитость плода, и более серьезные последствия. Не пугайтесь, ведь это происходит только в том случае, если данный диагноз оставить без внимания и не проводить лечение.
Незначительное нарушение, как правило, компенсируется за счет особенностей организма беременной женщины, однако при более серьезной патологии кровообращения происходит недостаточное снабжение малыша кислородом и питательными веществами. При таких обстоятельствах плод начинает недобирать в весе, происходит нарушение развития всех его органов, последствием чего может стать тяжелые роды, недоразвитость плода, и более серьезные последствия. Не пугайтесь, ведь это происходит только в том случае, если данный диагноз оставить без внимания и не проводить лечение.
Признаки и диагностика
Раннее старение эмбрионального органа всегда проходит бессимптомно для роженицы, а единственное, что может указывать на наличие этой болезни, это резкий упадок внутриутробной активности плода или, наоборот, ребенок будет вести себя чересчур активно. Как правило, данную патологию обнаружат на плановом УЗИ. При ультразвуковом исследовании может наблюдаться уменьшение площади и объема плаценты, что показывает несоответствие ее срокам развития. Для подтверждения диагноза обычно назначают дополнительные исследования, такие как ультразвуковая доплерография (позволяет получить информацию о нарушениях маточно-плацентарного кровотока). Дополнительно может быть проведена дополнительная кардиотокография, биохимическое и общее исследование крови.
Лечение
Лечение плацентарного старения осуществляется исключительно в условиях стационара под пристальным присмотром медицинских работников. Помимо комплексных мероприятий по нормализации кровотока и поддержания жизнедеятельности плода назначают лечение, направленное на устранение причины преждевременного старения плаценты. Так при обнаружении бактериальных, протозойных или вирусных инфекций назначаются различные медикаментозные препараты или инъекции для борьбы с ними. Чтобы предотвратить кислородное голодание ребенка назначают несколько разновидностей капельниц, а для нормализации кровотока применяют витаминотерапию и прописывают прием эссенциальных фосфолипидов, зуфилина, аспирина, актовегина, курантила и т. п.
п.
Как правило лечение преждевременного старения детского места ограничивается только лекарственными методами, однако в редких, более тяжелых случаях может быть проведено преждевременное родоразрешение. Но при этом врачи будут на 100% уверены, что развитие плода вне утробы матери принесет больше пользы, чем наличие возможных негативных последствий от преждевременных родов.
Недавние исследования показали, что если преждевременное старение (3 стадия) было выявлено на сроке больше 32 недель, то вероятность благоприятного исхода такая же, как и при здоровой беременности. Естественно, при этом необходима консультация врачей и регулярное УЗИ.
Степень зрелости плаценты: что нужно знать каждой беременной
2 января 2019 21:00 Елена НаумоваПлацента или «детское место» отвечает за развитие плода и связывает организм матери и ребенка. Что такое степень зрелости плаценты, как она изменяется и по каким критериям понять, что все в порядке?
Читайте такжеКрупный плод: причины и влияние на беременность и родыПлацента — это уникальный орган, который существует только во время беременности и отвечает за питание плода, защищает его от токсинов и вредных веществ, которые могут находиться в материнском организме. Зрелость плаценты меняется от срока беременности, со временем она становится толще, увеличивается количество кровеносных сосудов. Чем старее плацента, тем менее она способна справляться со своими основными функциями, но в норме, старение плаценты начинается после 36 недели и свидетельствует о приближающихся родах.
Какие степени зрелости плаценты существуют? Всего выделяют 4 степени зрелости плаценты:
- 0 — начальная стадия, длится примерно до 27-30 недель. «Юная» плацента способна нормально функционировать и обеспечивать плод необходимыми питательными веществами;
- 1 — промежуточная стадия, которая длится примерно с 27 по 34 неделю беременности;
- 2 — период зрелости, длится с 34 по 39 неделю беременности;
- 3 — старение, наступает примерно после 36 недели.

Состояние плаценты можно определить с помощью УЗИ, именно ультразвуковое исследование позволяет выявить на ней кисты и кальциевые отложение и, по необходимости, вовремя принять меры. Раннее старение плаценты чревато гипоксией плода, так как стареющая плацента не способна обеспечивать плод достаточным количеством кислорода и питательных веществ. Поэтому женщины, у которых наблюдается раннее старение плаценты, составляют группу риска и находятся под медицинским наблюдением. Чтобы понять, достаточно ли ребенку кислорода, беременной женщине назначают КТГ плода.
Причины раннего старения плаценты. Среди основных причин, которые провоцируют преждевременное старение плаценты выделяют:
- неправильное питание, в частности чрезмерное употребление кальция;
- гестоз;
- курение;
- резус-конфликт;
- эндокринные заболевания;
- травмы или инфекции матки;
- многоплодная беременность;
- предыдущие тяжелые роды или аборты;
- хронические заболевания почек, печени, сердца, сосудов.
Чем опасно раннее старение плаценты? Как мы уже говорили, старая плацента не может полностью справляться со своими функциями, это грозит ухудшением кровотока плода и, как следствие, гипоксией. Гипоксия может привести как к задержке внутриутробного развития плода, так и к его гибели, поэтому не стоит игнорировать плановый УЗИ и рекомендации врача. Плацентарная недостаточность лечится в условиях стационара и зависит от срока беременности. Помимо ультразвукового исследования, нужны дополнительные, среди которых, КТГ, допплер, биохимический анализ крови.
Важно прислушиваться к себе и ребенку, если вы заметили, что на протяжении некоторого временем малыш стал слишком активным или, наоборот, очень мало двигается, обязательно посетите своего акушера-гинеколога и опишите ему ситуацию. Будьте здоровы и легкой вам беременности!
Читайте такжеКанефрон при беременности: противопоказания, о которых важно знатьТакже обязательно узнайте о том, какие выделения во время беременности являются нормой, а когда нужно срочно обращаться к врачу
Фото в тексте: istockphoto. com
com
Как выявить преждевременное созревание плаценты
Титова Виктория Павловна Акушер-гинеколог, К.М.Н.,
Врач ультразвуковой диагностики
Что нужно знать о преждевременном старении плаценты?
Преждевременное созревание плаценты — это патология, при которой наблюдаются эхографические признаки зрелости плацентарной ткани, не соответствующие сроку беременности. Подобное осложнение выявляется при проведении планового скрининга. В рамках комплексной терапии патологии проводят лечение основного заболевания. Параллельно применяют препараты, предназначенные для улучшения кровообращения: сосудорасширяющие медикаменты, антиагреганты.
Причины, вызывающие патологию
Вероятность возникновения патологии увеличивается под воздействием перечисленных ниже факторов:- наличие у беременной женщины таких хронических заболеваний, как сахарный диабет, гипертоническая болезнь;
- аденомиоз;
- наличие у будущей матери эндометрита, протекающего в хронической форме;
- поздний токсикоз. При гестозе ухудшается кровоснабжение плода, ускоряется рост плаценты, что является причиной преждевременного созревания «детского места»;
- чрезмерная нагрузка на плацентарную ткань при наличии инфекционного заболевания;
- изосерологическая несовместимость беременной женщины и плода.
Симптомы заболевания
При преждевременном старении плаценты обычно превалируют симптомы основного заболевания. При явной плацентарной недостаточности изменяется двигательная активность будущего ребёнка. Шевеления плода становятся более частыми и интенсивными.
При явной плацентарной недостаточности изменяется двигательная активность будущего ребёнка. Шевеления плода становятся более частыми и интенсивными.
Методы диагностики
При подозрении на преждевременное старение плаценты проводится соответствующее ультразвуковое исследование. Диагностическая процедура помогает выявить:- толщину ткани плаценты;
- наличие структурных изменений;
- появление участков с нарушенным кровообращением.
- КТГ;
- фетометрия;
- фонокардиография.
Чем опасна неприятность?
Преждевременное старение плаценты может привести к появлению перечисленных ниже осложнений:- возникновение внутриутробной гипоксии плода;
- преждевременное излитие околоплодных вод;
- гибель плода;
- преждевременное начало родов;
- отслойка плаценты.
Лечение
В зависимости от характера заболевания, спровоцировавшего преждевременное старение плаценты, могут применяться:- антибиотики;
- препараты, содержащие гормоны;
- средства для лечения заболеваний, поражающих сердечно-сосудистую систему.
Помимо этого, при лечении заболевания могут применять эссенциальные фосфолипиды, антиагреганты. Беременной женщине следует нормализовать режим сна и отдыха, откорректировать питание, не забывать о рациональной двигательной активности.
Преждевременное старение плаценты при беременности: причины и лечение
1. Определение, функции и значение плаценты.
Определение
Плацента (с латинского «лепешка», или «детское место») – это орган, который развивается в организме беременной женщины и служит для обеспечения будущего ребенка в матке кислородом и питательными веществами, отвечая таким образом за его рост и развитие.
Плацента – связующее звено между организмами матери и ребенка, имеет форму диска, толщина которого к концу беременности составляет около 3 см, диаметр – около 20 см, вес около 0,5 кг. Одной стороной плацента прикреплена к матке, то есть она расположена в матке. Состоит плацента из долек, которые, в свою очередь, содержат капиллярные сосуды. Другой своей стороной плацента обращена к плоду и соединена с ним пуповиной. В пуповине находится три сосуда: по венозному течет артериальная кровь, по двум артериальным – венозная. Несмотря на тесную связь, кровь плода никогда не смешивается с кровью матери.
Функции
Плацента выполняет следующие функции:
- Обеспечивает питание плода, а, значит, его рост и развитие.
- Осуществляет газообмен – доставляет к плоду кислород, и выводит от него углекислый газ.
- Защищает плод от инфекций с помощью плацентарного барьера, через который ряд веществ проникнуть не может ввиду своего размера или структуры.
- Вырабатывает гормоны, поддерживая беременность.
- Участвует в формировании будущего иммунитета ребенка.
Исходя из функций плаценты, понятно, что любые изменения в работе и состоянии плаценты оказывают влияние на мать и на ребенка. Повреждение плаценты влечет за собой недостаток питания плода, нарушение его развития, а в некоторых случаях – его гибель.
Значение
Плацента образуется к концу второй недели беременности, когда оплодотворенная яйцеклетка внедрилась в стенку матки. До тех пор зародыш питается самостоятельно и не зависит от питания и образа жизни матери. После того как сформировалась плацента, образовалась связь между матерью и будущим ребенком и все вещества, поступающие в организм матери, в том числе алкоголь, никотин, лекарственные препараты, будут проникать и в зародыш. На этом этапе будущей матери стоит задуматься, пересмотреть свой рацион, отказаться от вредных привычек, чтобы впоследствии родить здорового малыша. Значение плаценты трудно переоценить.
На этом этапе будущей матери стоит задуматься, пересмотреть свой рацион, отказаться от вредных привычек, чтобы впоследствии родить здорового малыша. Значение плаценты трудно переоценить.
2. Степени зрелости плаценты.
На протяжении всей беременности плацента растет и изменяется.
В акушерстве выделяют 4 степени (стадии) зрелости плаценты:
0 – соответствует 13-19 неделям беременности – стадия формирования плаценты;
1 – 20-31 неделям – стадия роста плаценты;
2 – 32-37 неделям – стадия зрелости плаценты;
3 – 38-41 неделям – стадия естественного старения плаценты.
В норме «детское место» полностью формируется к концу первого триместра беременности, но растет на протяжении всего срока беременности вместе с ростом матки и будущего ребенка, и старение плаценты происходит ближе к родам.
Для каждой степени характерны определенные размеры, структура, вид плаценты. Если тот или иной параметр не соответствует норме, говорят о преждевременном старении плаценты. То есть если признаки, характерные для плаценты 2-ой степени зрелости, выявлены до 32 недель, или признаки 3-ей степени – до 38 недель. Вывод о раннем старении плаценты делает врач, проведя УЗИ-диагностику плаценты, измерив ее толщину, оценив состояние.
Преждевременное старение плаценты приводит к тому, что площадь ее поверхности уменьшается, на отдельных участках откладываются соли. Здесь стоит сказать, что часто разные врачи используют различные критерии оценки состояния плаценты. Поэтому следует обращаться к проверенному врачу, имеющему хорошую репутацию, квалификацию и опыт.
3. Причины, признаки, последствия и лечение преждевременного старения плаценты.
Причины
Причиной раннего старения плаценты могут быть различные заболевания будущей матери. Например, сахарный диабет, гипертензии во время беременности, сердечно-сосудистые заболевания, болезни печени, почек, мочевыводящих путей, бронхиальная астма, ВИЧ-инфекция, вирусные заболевания в течение беременности, недостаточная или избыточная масса тела женщины. Также раннее старение плаценты может начаться из-за сложностей, возникающих при беременности:
Также раннее старение плаценты может начаться из-за сложностей, возникающих при беременности:
- наследственные патологии плода,
- задержка внутриутробного развития,
- резус-конфликт,
- отслойка плаценты и ее неправильное прикрепление,
- многоплодная беременность,
- токсикоз на поздних сроках беременности,
- многоводие,
- маловодие,
- нарушение свертываемости крови.
Неправильный образ жизни беременной женщины, курение, употребление алкоголя, наркотических препаратов, некоторых лекарственных средств, повреждения матки вследствие абортов, сложные предыдущие роды также могут повлечь за собой преждевременное старение плаценты. Причин может быть сразу несколько.
Очевидно, что в зону риска попадает достаточно много женщин, можно сказать, большинство.
Поэтому женщины, имеющие какие-либо заболевания из вышеперечисленных или осложнения во время беременности, перенесшие в прошлом аборты и трудные роды должны обязательно тщательно наблюдаться у врача, выполнять все требования, проходить все необходимые обследования. Вовремя поставленный диагноз и обнаруженная его причина – это уже начало лечения и залог рождения здорового ребенка.
Признаки, последствия и лечение
Явных признаков раннего старения плаценты нет. Последствиями такого диагноза в первом триместре беременности может стать «замершая» беременность, возникновение пороков развития, во втором или третьем – гипоксия плода, то есть недостаточное питание плода кислородом, вызывающее повреждение всех органов, а больше всего – головного мозга. На поздних сроках такая патология плаценты может привести к раннему отхождению околоплодных вод, отслоению плаценты. Чаще всего при таком диагнозе рождаются дети с малым весом.
Если поставлен диагноз «преждевременное старение плаценты», не нужно впадать в отчаяние. Иногда диагноз выставляется неверно, преждевременно.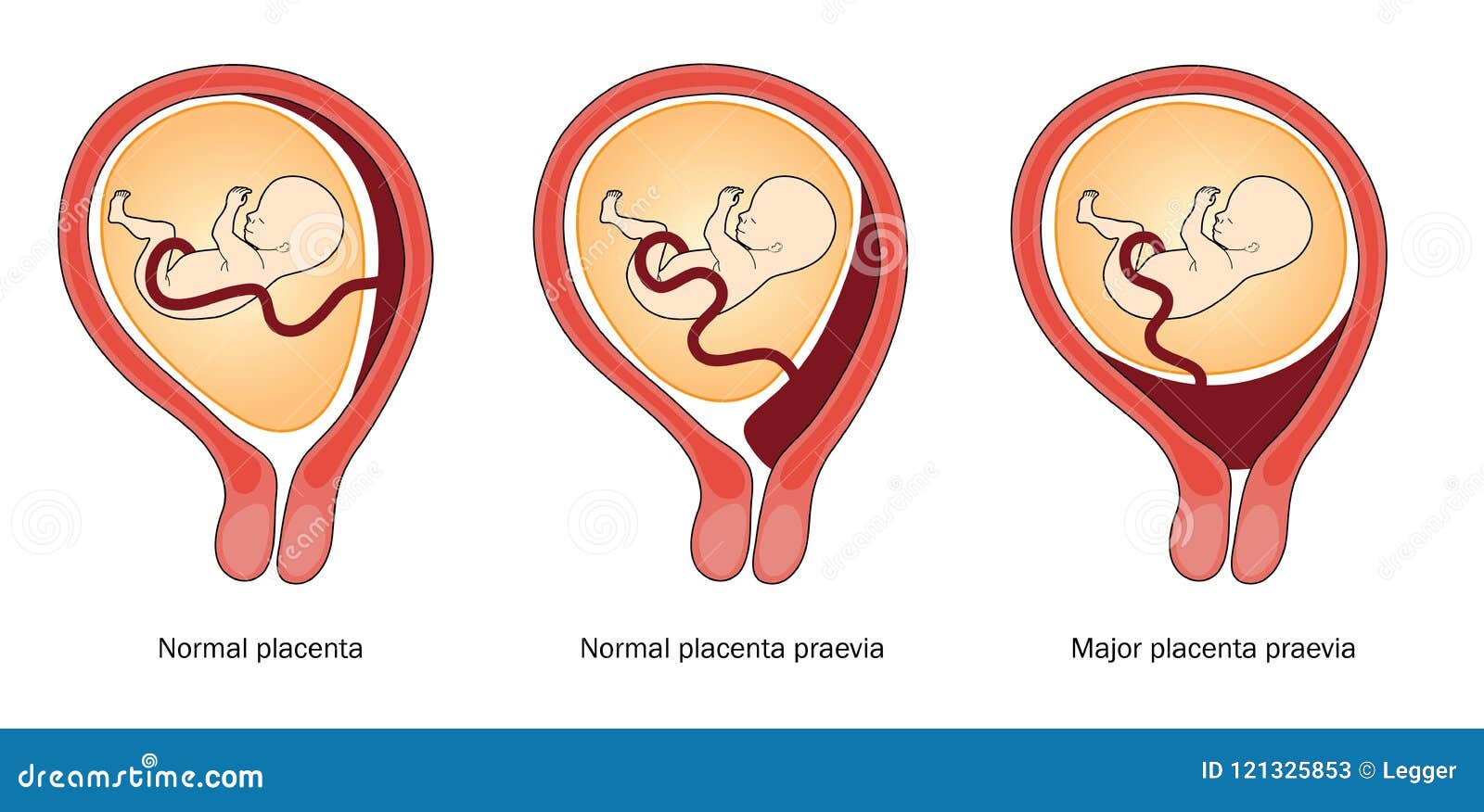 Необходимо провести дополнительные исследования – УЗИ, кардиотокография (КТГ), тест на эстроген, более тщательное наблюдение. С помощью УЗИ исследуют кровоток, идущий от матери к ребенку через плаценту. КТГ исследует частоту сердечных сокращений плода, его двигательную активность. Уровень эстрогена в крови матери сравнивают с нормой и делают вывод о достаточности или недостаточности работы плаценты.
Необходимо провести дополнительные исследования – УЗИ, кардиотокография (КТГ), тест на эстроген, более тщательное наблюдение. С помощью УЗИ исследуют кровоток, идущий от матери к ребенку через плаценту. КТГ исследует частоту сердечных сокращений плода, его двигательную активность. Уровень эстрогена в крови матери сравнивают с нормой и делают вывод о достаточности или недостаточности работы плаценты.
Вылечить саму плаценту невозможно, процесс старения плаценты необратим. Необходимо определить состояние плода с помощью УЗИ, КТГ и доплерографии. Если выявляется отставание в развитии будущего ребенка, женщине необходимо стационарное лечение. При лечении раннего старения плаценты применяются препараты, улучшающие дыхание плода («Курантил», «Актовегин», «Эссенциале»), глюкоза и препараты, снижающие тонус матки. Если причиной стала какая-либо инфекция беременной женщины, одновременно назначаются специальные препараты для ее лечения. Лечение чаще всего проводится в условиях стационара, ни в коем случае нельзя от него отказываться.
В крайних случаях, если лечение не дает положительной динамики и плод страдает, прибегают к родовозбуждению до окончания срока беременности.
Автор статьи: Кунцевич Ирина Васильевна
Преждевременное старение плаценты: раннее созревание при беременности, причины на 32 и неделе последствия
Плацента формируется в процессе беременности. Именно от нее зависит выработка гормонов, достаточное поступление кислорода к плоду, и питательных веществ. Существует определенная схема созревания плаценты, которую заложила природа. Преждевременное старение плаценты оказывает негативные последствия на здоровье плода и будущей матери.
- Преждевременное созревание плаценты
- Старение плаценты: стадии
- Причины старения плаценты при беременности и что делать
- Ранее созревание плаценты: почему и у кого
- Лечение преждевременного созревания плаценты: 32 недели беременности
- Причины преждевременного старение плаценты (видео)
Преждевременное созревание плаценты
Плацента обеспечивает функции питания кровообращения и дыхания ребенка. У малыша эти процессы не могут происходить самостоятельно, пока не сформируются все органы. Функции дыхания и питания происходят при поддержке матери. Плацента обеспечивает защиту малыша от различных инфекций.
У малыша эти процессы не могут происходить самостоятельно, пока не сформируются все органы. Функции дыхания и питания происходят при поддержке матери. Плацента обеспечивает защиту малыша от различных инфекций.
Плацента, как и другие органы в нашем организме, стареет и к 37 недели беременности готовится выйти из организма.
Но часто при легкомысленном отношении женщины к своему здоровью во время беременности происходит раннее созревание плаценты. Развитие этого органа раньше времени, является патологией, и влечет за собой различные последствия. Если плацента начинает созревать немного раньше срока, это еще не означает, что ситуация критична. Это может быть связано с особенностями организма женщины. В случае если плацента созревает до 36 недель, это говорит о раннем созревании, которое необходимо остановить.
Ускоренное созревание плаценты грозит:
- Недостатком кислорода,
- Недостатком питательных веществ,
- Отслоением плаценты,
- Не исключено прерывание беременности.
Недостаточное поступление кислорода и питательных веществ, зачастую приводит к малому весу ребенка, гипоксии. Стареющая раньше времени плацента может привести к рождению ребенка с патологиями головного мозга, к повреждению органов матери или ребенка. Случается, что приводит к летальному исходу. Чтобы предотвратить такие последствия, надо вовремя остановить преждевременное созревание плаценты.
Старение плаценты: стадии
Созревание и старение плаценты – процесс естественный. О патологии этого процесса можно говорить, если плацента начинает стареть раньше положенного срока. Старение этого органа приводит к снижению его функций. Плацента второй степени зрелости прекращает рост, и не может обеспечить кислород и питательные вещества ребенку в полной мере в процессе его развития. Признаки преждевременного старения диагностируются УЗИ и КТГ.
Развитие плаценты проходит четыре стадии:
- Плацента формируется со 2 по 30 неделю,
- С 30 по 33 неделю происходит рост,
- С 34 по 36 неделю плацента созревает,
- На 37 недели плацента стареет.

В некоторых случаях слишком быстрого старения плаценты, врачи могут посоветовать прервать беременность.
Причины старения плаценты при беременности и что делать
Причины возникновения патологии развития плаценты у беременных могут быть самыми различными. Это может быть индивидуальная особенность организма беременной женщины, или влияния на плаценту каких-либо патологий, и инфекций.
Распространенные причины старения плаценты:
- Заболевание эндокринной системы,
- Заболевания почек, печени,
- Алкоголь,
- Курение,
- Инфекции половых органов и матки,
- Сильный токсикоз,
- Лишний вес,
- Сделанные ранее аборты, или перенесенные тяжелые роды.
Плацента трудится для защиты ребенка от негативных внешних воздействий. При неправильном питании матери, плаценте приходится защищать плод от вредных веществ с удвоенной силой. Это приводит к более быстрому развитию плаценты, и старению раньше положенного. Такое развитие происходит так же из-за курения, употребления алкоголя, если плаценте приходится защищать плод от инфекций. Инфекционные заболевания могут привести помимо старения плаценты, к многоводию или маловодию.
Ранее созревание плаценты: почему и у кого
Раннее созревание плаценты диагностируется ультразвуковым исследованием, и диагноз определяется исключительно по данным УЗИ. Если степень созревания плаценты не соответствует срокам беременности, значит, происходит быстрое созревание, и в следствии старение плаценты.
В случае если по результатам УЗИ определили диагноз раннего созревания, не следует раньше времени паниковать.
Раннее созревание плаценты не всегда говорит о каких-либо патологиях. Нужно пройти лечение, которое поможет нормализовать нормальный кровоток, и следить за состоянием ребенка по КТГ. В первые месяцы беременности раннее созревание плаценты может привести к прерыванию беременности или отклонениям у ребенка.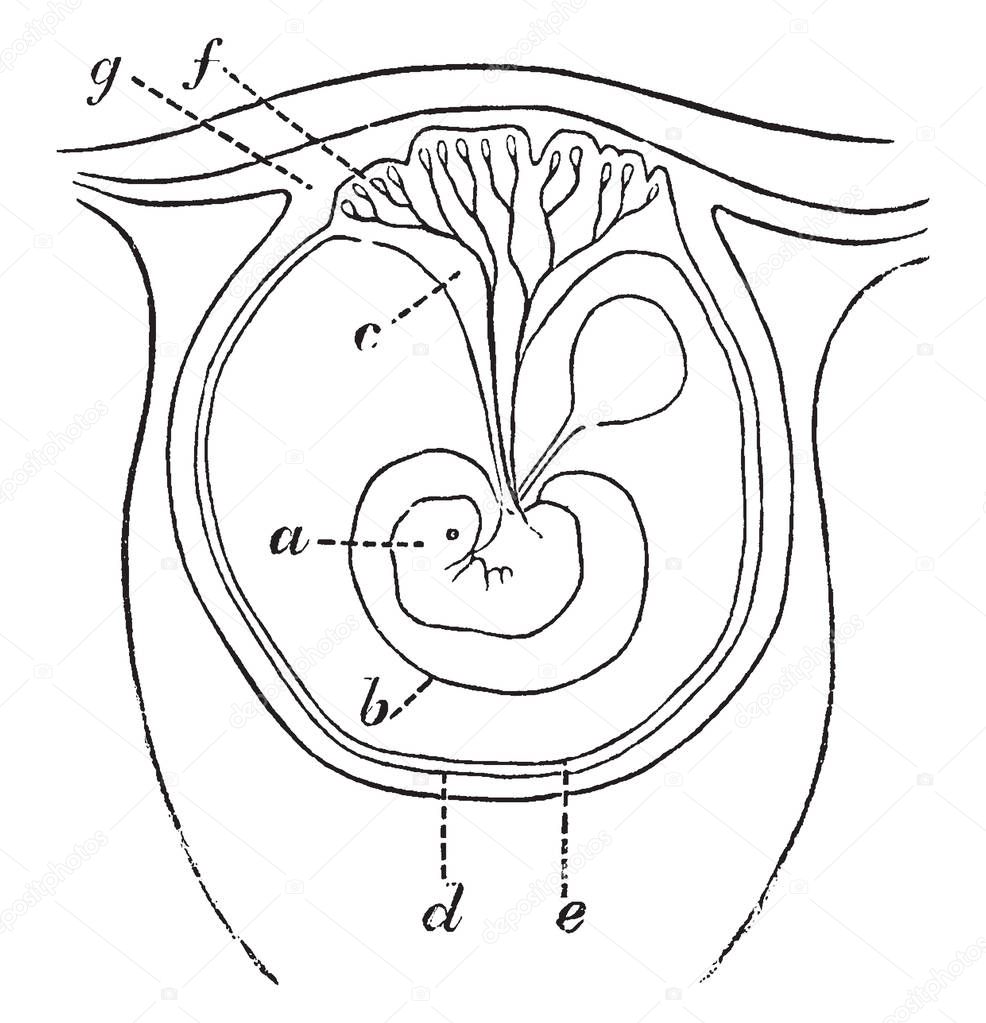 Из-за недостатка кислорода возможно отмирание клеток головного мозга. Также может привести к раннему отслоению плаценты.
Из-за недостатка кислорода возможно отмирание клеток головного мозга. Также может привести к раннему отслоению плаценты.
Раннее созревание плаценты вызывает кислородное голодание у малыша. Сердце ребенка начинает учащенно работать, чтобы ускорить кровоток, и обеспечить ткани кислородом. В этом случае ребенок начинает проявлять резкую активность, или наоборот затихает. Такие проявления должны насторожить женщину.
Если диагноз раннее созревание поставили вовремя и назначили соответствующее лечение, то преждевременное созревание не грозит ни ребенку, ни матери. Опасно если допустить фетоплацентарную недостаточность. Это приводит к тяжелым последствиям.
Лечение преждевременного созревания плаценты: 32 недели беременности
На сроке 32 недели беременности малыш заметно прибавляет в весе и росте. Его развитие во многом зависит от наследственности, передающейся от родителей. В этот период, при условии нормального развития плацента прекращает свой рост и через месяц начинает стареть.
Но если на 32 неделе достигается третья степень созревания плаценты, то можно говорить, что происходит преждевременное старение.
Симптомы, по которым можно определить преждевременное созревание плаценты не проявляются. Самостоятельно понять, что развитие плаценты не соответствует срокам беременности не возможно. Эти признаки выявляют только УЗИ и КТГ. По результатам УЗИ делают вывод о нехватке ребенку кислорода и питательных веществ. Назначают анализы на инфекции. Препараты для лечения назначают, если состояние ребенка ухудшилось.
Лечение проводят только в стационаре. Прием препаратов и капельниц проходит под контролем врачей. Именно при госпитализации можно оказать помощь в полном объеме. Преждевременное созревание плаценты часто дает основание для родов с медицинской помощью, и раньше положенного срока. Если врачи опасаются за здоровье ребенка, они могут вынести решение о родах путем кесарева сечения досрочно.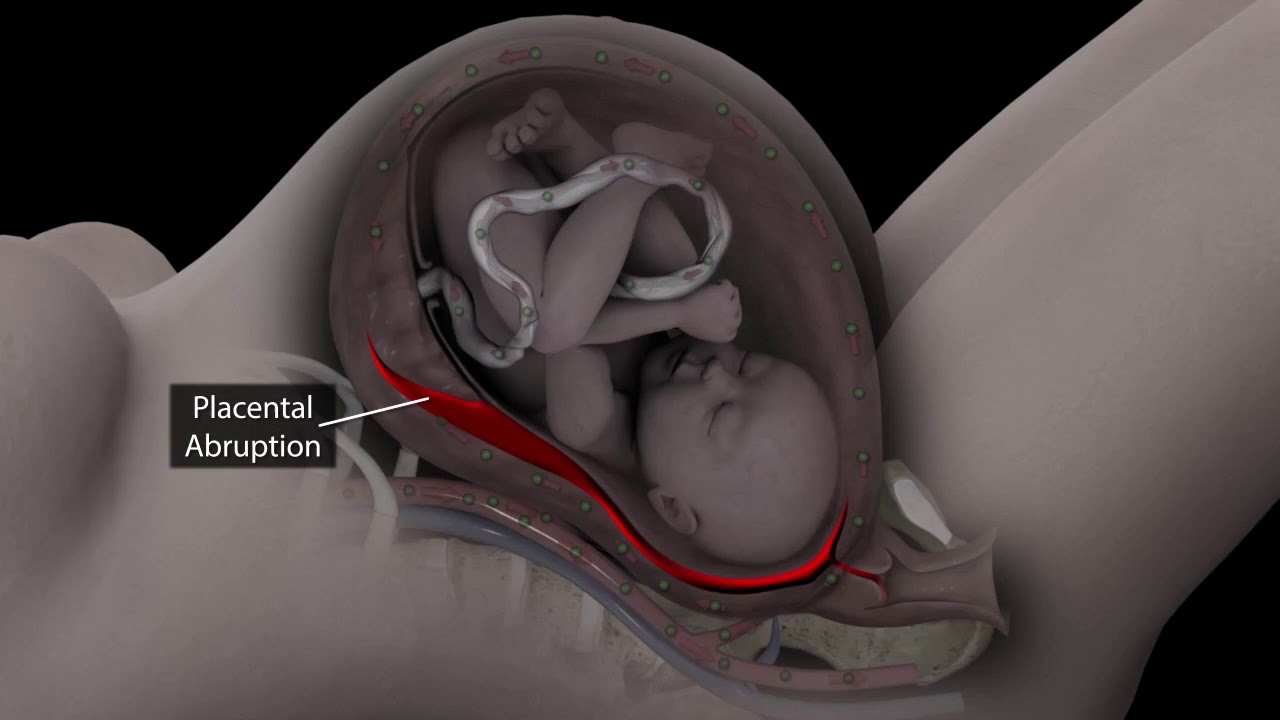
Если диагноз не поставить вовремя и не назначить лечение, преждевременное старение может привести к тому, что ребенок может задохнуться от нехватки кислорода. Определенной схемы лечения преждевременной зрелости плаценты нет. При лечении как правило назначают витамины, покой, и устраняют причины, приведшие к преждевременному созреванию плаценты. Назначают такое лекарство как Актовегин и Курантил. Вылечить плаценту не возможно. Назначенное лечение направлено на поддержание плаценты, чтобы облегчить ее работу и наладить кровообращение.
Вовремя принятые меры, и соблюдение всех рекомендаций помогает родить здорового ребенка в срок, и избежать последствий преждевременного старения плаценты.
Во время беременности плацента созревает, развивается, стареет. Это все естественные процессы. Но если развитие плаценты не соответствует срокам беременности, это заслуживает особого внимания. Исследования кровотока современными методами позволяют провести точную диагностику и поставить своевременный диагноз. Благодаря этому результаты лечения становятся более выше, а выбранная тактика ведения беременности, если плацента старая, позволяет добиться наиболее благоприятного завершения беременности и родов.
Причины преждевременного старение плаценты (видео)
Раннее старение плаценты может начаться и на поздних сроках беременности. Если этот процесс происходит не слишком быстро, то беременность заканчивается рождением ребенка естественным способом с небольшим весом. Если старение плаценты происходит слишком быстро, то врачи могут решить произвести роды путем кесарева сечения. Такое решение принимается в случае если необходимо сохранить жизнь и здоровье ребенка. Очень важна профилактика.
Загрузка…Укорочение теломер, старение клеток и дисфункция митохондрий
Преэклампсия — мультисистемное заболевание беременности и основная причина материнской и неонатальной заболеваемости и смертности во всем мире. Точная патофизиология преэклампсии остается неясной; однако предполагается, что различные патологии могут быть связаны с нарушением ремоделирования сосудов и повышенным окислительным стрессом в плаценте. Окислительный стресс играет ключевую роль в старении клеток, а постоянное присутствие повышенного окислительного стресса ускоряет клеточное старение и дисфункцию митохондрий, что приводит к преждевременному старению плаценты.Преждевременное старение плаценты связано с плацентарной недостаточностью, которая снижает функциональные возможности этого важного органа и приводит к аномальным исходам беременности. Изменения, вызванные окислительным воздействием, необратимы и часто приводят к вредным модификациям макромолекул, таких как липиды и белки, мутациям ДНК и изменению функционирования и динамики митохондрий. В этом обзоре мы обобщили текущие знания о старении плаценты в этиологии неблагоприятных исходов беременности и обсудили признаки старения, которые могут быть потенциальными маркерами преэклампсии и задержки роста плода.
Точная патофизиология преэклампсии остается неясной; однако предполагается, что различные патологии могут быть связаны с нарушением ремоделирования сосудов и повышенным окислительным стрессом в плаценте. Окислительный стресс играет ключевую роль в старении клеток, а постоянное присутствие повышенного окислительного стресса ускоряет клеточное старение и дисфункцию митохондрий, что приводит к преждевременному старению плаценты.Преждевременное старение плаценты связано с плацентарной недостаточностью, которая снижает функциональные возможности этого важного органа и приводит к аномальным исходам беременности. Изменения, вызванные окислительным воздействием, необратимы и часто приводят к вредным модификациям макромолекул, таких как липиды и белки, мутациям ДНК и изменению функционирования и динамики митохондрий. В этом обзоре мы обобщили текущие знания о старении плаценты в этиологии неблагоприятных исходов беременности и обсудили признаки старения, которые могут быть потенциальными маркерами преэклампсии и задержки роста плода.
1. Введение
Преэклампсию можно определить как гипертензию de novo после 20 недель беременности при наличии протеинурии и дисфункции материнского органа / маточно-плацентарной [1]. Это одна из основных причин материнской и неонатальной заболеваемости и смертности, от которой страдает от 3 до 8% беременностей во всем мире [2]. Преждевременные роды в результате ятрогенных родов являются частым фактором преэклампсии, при этом до 25% детей, рожденных от преэклампсических матерей, имеют задержку роста [2, 3].Преэклампсия и ЗВУР — специфические для беременности расстройства, связанные с плацентарной недостаточностью [4]. Осложнения, связанные с преэклампсией, являются причиной около 15% материнской смертности и высоких показателей перинатальной смертности во всем мире [5]. Органы неизбежно переживают старение; однако при преэклампсии наличие стойкого окислительного стресса ускоряет этот процесс, что приводит к преждевременному старению плаценты [6]. В различных исследованиях сообщалось, что преждевременное старение плаценты связано с укорочением теломер, клеточным старением и дисфункцией митохондрий [7-10].
В различных исследованиях сообщалось, что преждевременное старение плаценты связано с укорочением теломер, клеточным старением и дисфункцией митохондрий [7-10].
2. Физиология старения
Старение — это однонаправленное явление, которое неизбежно испытывает каждая ткань. Его можно охарактеризовать как клеточное старение из-за снижения функциональности и дисфункции митохондрий из-за изменения метаболизма и передачи сигналов.
2.1. Cellular Senescence
Клетки способны к репликации, делясь на две точные копии родительской клетки. Это включает в себя разделение генетического материала путем раскручивания и расщепления цепей ДНК с образованием двух новых копий в качестве дочерних цепей.Теломеры представляют собой кэп-подобные нуклеотидные повторы (TTAGGG), присутствующие на конце каждой цепи. Повреждение цепей ДНК активирует сигнальные каскады (мутантная атаксия, телеангиэктазия (ATM) и атаксия, телеангиэктазия и Rad3-связанные пути (ATR)), которые останавливают деление клеток, вызывают клеточное старение и способствуют гибели клеток [11]. Теломеры с другими белками, такими как шелтерин, защищают конец ядер от распознавания как двухцепочечный поврежденный участок (DDR) [11]. Было показано, что теломеры укорачиваются после каждого цикла репликации [12].С увеличением пролиферации и уменьшением размера теломер клетки вступают в фазу старения или задержки роста (предел Хейфлика), что в конечном итоге приводит к гибели клеток [12]. Укорочение теломер было связано с различными генетическими заболеваниями, такими как прогерия, преждевременное старение и синдром Хатчинсона-Гилфорда [13].
В некоторых случаях, например, при раке, клетки могут обходить старение и продолжать размножаться, становясь бессмертными. Однако даже раковые клетки не делятся бесконечно и вступают в стадию кризиса, которая приводит либо к гибели клеток, либо к стабилизации длины теломер с последующей активацией фермента теломеразы для поддержания длины теломер [14].Теломераза представляет собой комплекс РНК-белок, который восполняет потерянные нуклеотиды для сохранения длины теломер [15].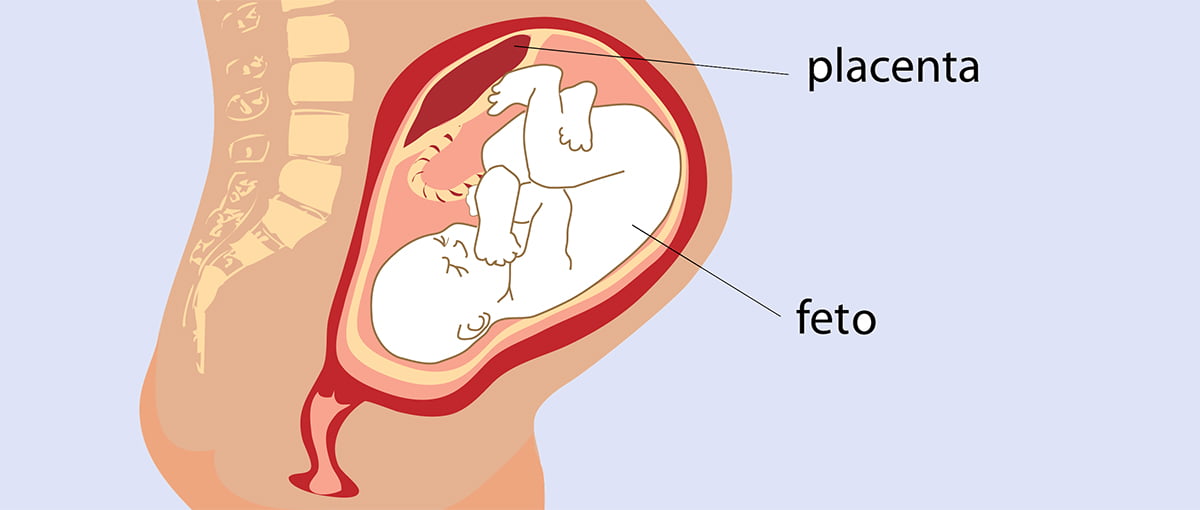 В соматических клетках теломеразы отключены как защитный механизм для предотвращения неопластических изменений [16], но их активность более выражена в половых клетках, стволовых клетках и 90% раковых клеток [17].
В соматических клетках теломеразы отключены как защитный механизм для предотвращения неопластических изменений [16], но их активность более выражена в половых клетках, стволовых клетках и 90% раковых клеток [17].
2.2. Дисфункция митохондрий
Митохондрии являются ключевыми регуляторами метаболизма, окислительно-восстановительного баланса и апоптоза. Во время цепи переноса электронов (ETC) электроны перекачиваются через внутреннюю мембрану митохондрий (от восстановленных соединений до молекулярного кислорода), создавая отток для синтеза энергии [18].Согласно гипотезе старения, основанной на свободных радикалах или окислительном стрессе, во время окислительного фосфорилирования происходит ряд событий временной шкалы, приводящих к выщелачиванию электронов из митохондриальных мембран, которые вступают в реакцию с кислородом, образуя свободные радикалы, такие как супероксид, что в конечном итоге нарушает окислительно-восстановительный баланс [19, 20]. На смену теории свободных радикалов пришла гипотеза теории повреждений, которая предполагает, что старение может быть связано с частым и неизбежным кумулятивным повреждением на молекулярном уровне, вызванным накоплением активных форм кислорода (АФК), его побочными продуктами и ферментами [21].Накопление активных форм кислорода (АФК) приводит к обратимым и необратимым изменениям в клетках, что приводит к потере молекулярного функционирования и усилению окислительного стресса — феномену, часто связанному со старением, как показано на Рисунке 1 [19, 20].
Функционирование митохондрий при старении широко изучено; в ряде статей сообщалось, что плотность митохондрий, дыхательная способность и продукция АТФ снижаются с клеточным старением [22–24].Помимо снижения функциональности, старение сопровождается повреждением митохондриальной ДНК (мтДНК), мутациями и митофагией [22, 25].
Нарушение окислительно-восстановительной передачи сигналов вызывает различные модификации внутри макромолекул и мутации внутри мтДНК; однако вредные эффекты этих мутаций мтДНК до сих пор полностью не выяснены [26–28].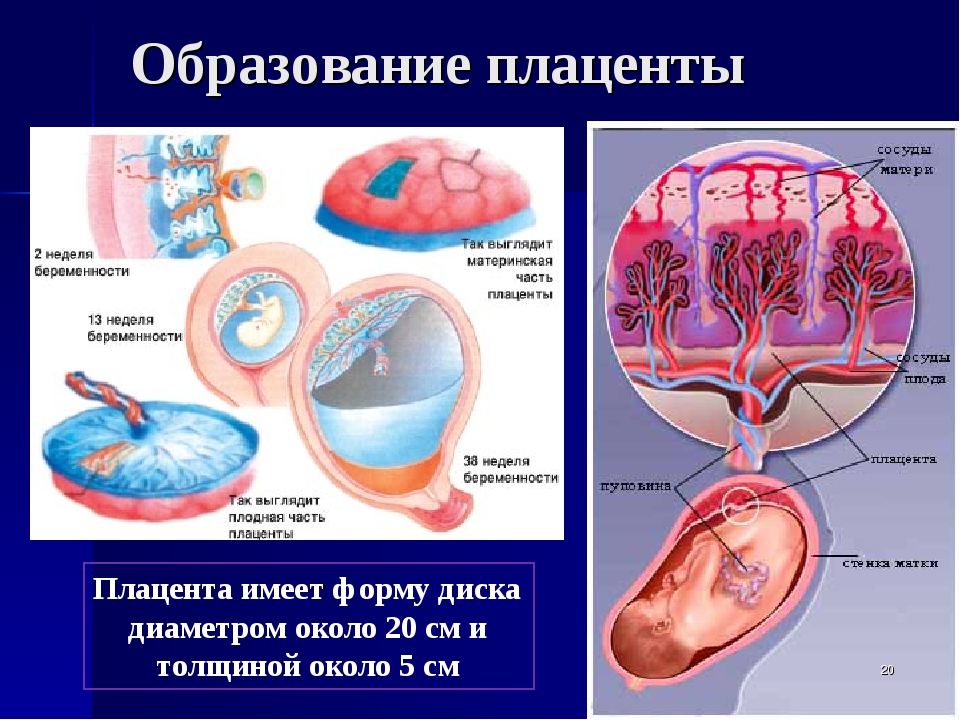 Эффект бутылочного горлышка, который объясняет генетические дрейфы и вариации в небольших популяциях, как в случае с мутациями мтДНК, может передавать небольшие вариации в зародышевых линиях, которые усиливаются на более поздних стадиях оогенеза [29, 30].В нескольких исследованиях сообщается, что мутации в мтДНК дрожжей приводят к сокращению продолжительности жизни при ингибировании митофагии [31, 32]. Уменьшение количества копий мтДНК было связано со старением и связанными с ним заболеваниями, включая сердечно-сосудистые заболевания (кардиомиопатия, атеросклероз), нейродегенеративные заболевания (болезнь Альцгеймера, болезнь Паркинсона), рак и преждевременное старение яичников у женщин [33, 34].
Эффект бутылочного горлышка, который объясняет генетические дрейфы и вариации в небольших популяциях, как в случае с мутациями мтДНК, может передавать небольшие вариации в зародышевых линиях, которые усиливаются на более поздних стадиях оогенеза [29, 30].В нескольких исследованиях сообщается, что мутации в мтДНК дрожжей приводят к сокращению продолжительности жизни при ингибировании митофагии [31, 32]. Уменьшение количества копий мтДНК было связано со старением и связанными с ним заболеваниями, включая сердечно-сосудистые заболевания (кардиомиопатия, атеросклероз), нейродегенеративные заболевания (болезнь Альцгеймера, болезнь Паркинсона), рак и преждевременное старение яичников у женщин [33, 34].
Митофагия — это защитный механизм для поддержания качества митохондрий, удаления мутированной мтДНК и обеспечения митохондриального гомеостаза [35].Более того, митохондриальная динамика поддерживается за счет частого деления и слияния митохондрий [36]. Окислительное повреждение митохондрий может вызвать нарушение деления с асимметричными мембранными потенциалами дочерних митохондрий, которые не могут эффективно слиться, что приводит к накоплению деформированных митохондриальных белков со сниженной аутофагической способностью [37]. Паликарас и др. показали, что митофагия необходима для долголетия у C. elegans в результате снижения передачи сигналов инсулина / IGF-1 или нарушения функции митохондрий [38].
Кроме того, потеря митохондриального биогенеза из-за дисбаланса митофагии и митохондриального деления / слияния и накопления митохондриального мусора приводит к старению сердца у мышей [39, 40].
Нарушение функции митохондрий отражает ответ митохондриального развернутого белка (UPR mt ) [41], который регулируется связью между митохондриальными и ядерными белками, где ядерное ремоделирование требуется для активации UPR mt [42].Когда внутри клеток индуцируется стресс, UPR mt активируется, чтобы способствовать репарации, но в случаях пролонгированного действия UPR mt могут индуцироваться мутации внутри мтДНК [42]. Эксперименты на C. elegans показали, что активация UPR mt и дисбаланс митонуклеарного ответа вызывают долголетие [43, 44].
Эксперименты на C. elegans показали, что активация UPR mt и дисбаланс митонуклеарного ответа вызывают долголетие [43, 44].
Клеточное старение является результатом повреждения ядра, обычно связанного с высоким окислительным стрессом и накоплением АФК, остатков или неправильно свернутых белков.Врожденные иммунные медиаторы с секреторными фенотипами, ассоциированными со старением (SASP), включая цитокины, хемокины, факторы роста и протеазы, ответственны за удаление дебриса из мертвых или умирающих клеток, которые могут активировать проапоптотические пути передачи сигналов p53 и AKT [45–47]. В нескольких исследованиях удаление медиаторов воспаления и последующая передача сигналов вызывали обратное развитие клеточного старения, указывая на то, что воспаление может быть как причиной, так и следствием клеточного старения [48–50].
3.Патофизиология преэклампсии
Патофизиология преэклампсии, даже после десятилетий исследований, до конца не изучена. Преэклампсию можно охарактеризовать как раннее начало, составляющее менее 20% всех случаев, или как позднее начало, составляющее оставшиеся 80% [51]. Было предложено несколько гипотез, чтобы полностью выяснить лежащие в основе патологические механизмы [51–54]. Плацентарное происхождение гипотезы преэклампсии описывает неэффективную инвазию трофобластов и ремоделирование спиральных артерий матери, вызывающее «плацентарный синдром», впоследствии приводящее к преэклампсии и задержке роста плода [51, 54].
Более поздняя теория, предложенная Thilaganathan, предполагает, что аномальная сердечно-сосудистая функция вызывает аномальную плаценту, которая возникает при преэклампсии, а плацентарное происхождение преэклампсии справедливо только в случае раннего начала заболевания [52, 54]. Позднее начало преэклампсии может быть связано с основной сердечно-сосудистой дисфункцией матери, которая не может удовлетворить гемодинамические и метаболические потребности беременности, а также приводит к неблагоприятным послеродовым сердечно-сосудистым исходам у более чем 50% пациентов, возможно, из-за того, что преэклампсия и сердечно-сосудистые заболевания имеют сходные генетические факторы и факторы риска окружающей среды [52].
Подтверждая связь между плацентарной патофизиологией ранней ПЭ, Yung et al. исследовали образцы плаценты от преждевременных, доношенных беременностей и беременностей во втором триместре и продемонстрировали, что при преэклампсии с ранним началом патология плаценты связана с активацией пути развернутого белкового ответа (UPR) и активацией стресса ER наряду с угнетением пути AKT, снижая клеточную активность. распространение [55]. Эти авторы продемонстрировали молекулярные различия между двумя фенотипами доношенной преэклампсии и преэклампсии [55].
Робертс и Хьюбел, среди прочих, предложили двухэтапную модель преэклампсии, которая позже была изменена на шесть стадий Redman et al. [53, 56]. Редман объясняет, что стадии 1 и 2 могут быть ранним явлением, таким как предубежденная толерантность матери к отцовской сперме или короткий промежуток времени между коитусом и зачатием, что приводит к плохой плацентации и влияет на здоровье и рост плода [53]. Стадия 3 начинается примерно на 8 неделе беременности, когда в неосложненных случаях трофобластические пробки, закрывающие спиральные артерии матери, отступают и начинается маточно-плацентарное кровообращение [53, 57].Однако при преэклампсии происходит преждевременное открытие трофобластических пробок с притоком артериальной крови, увеличивающим стресс внутри плаценты и приводящим к дефектной плаценте [53]. Стадия 4 модели Редмана характеризуется снижением факторов роста плаценты в случаях преэклампсии, что приводит к нарушению ремоделирования сосудов материнских спиральных артерий в более крупные сосуды с низким сопротивлением току крови трофобластом [53, 58, 59]. Кроме того, Redman также заявляет, что при увеличении плацентарного и эндотелиального повреждения клинические симптомы преэклампсии проявляются на стадиях 5 и 6 [53].
Развитие плаценты начинается с децидуальной реакции, вызванной бластоцистой в материнском эндометрии, что в конечном итоге приводит к образованию базальной пластинки [60, 61]. Трофобласты дифференцируются на два типа: инвазивный вневорсинчатый цитотрофобласт (EVT) или ворсинчатый цитотрофобласт, который позже сливается с образованием многоядерного синцитиотрофобласта [61, 62]. Экстраворсинчатые цитотрофобласты ответственны за установление маточно-плацентарного кровообращения и регуляцию материнской врожденной иммунной системы [63, 64].При неосложненной беременности вневорсинчатые цитотрофобласты (EVT) вторгаются в спиральные артерии, вены и лимфатические сосуды эндометрия матери в течение первого триместра [65, 66]. Накопления EVT также локализовались в лимфатических узлах без каких-либо неопластических изменений, что указывает на регуляцию иммунных клеток трофобластами [65, 66].
Дефектная плацентация приводит к снижению ангиогенного фактора роста эндотелия сосудов (VEGF) и фактора роста плаценты (PLGF) и высвобождению вредных факторов плаценты, таких как растворимая fms-подобная тирозинкиназа 1 (sFIt1), в кровоток матери, вызывая генерализованный эндотелиальный дисфункция [56, 57].Циркулирующий sFlt1 широко распространен у женщин с преэклампсией, что объясняется сосудистым сопротивлением и повышением артериального давления [67]. Недавние исследования у женщин с задержкой роста плода (FGR) без симптомов преэклампсии предоставили доказательства высокого отношения sFlt1 / PLGF [68, 69]. Протеинурия при преэклампсии также может быть связана с высокими уровнями плацентарных факторов, таких как sFlt1, ускоряющих гломерулярный эндотелиоз [70]. Измененная гемодинамика и снижение сосудистого кровотока приводят к стойким состояниям гипоксии и оксигенации, что приводит к высокому окислительному стрессу в тканях плаценты [55, 71–74].Несмотря на то, что повышенный окислительный стресс проявляется в трофобластах при неосложненной беременности, длительный окислительный стресс подавляет активность трофобластов, ухудшая ситуацию с осложнениями беременности [75].
Синцитиотрофобласт — это самый внешний слой ворсинчатого трофобласта, находящийся в прямом контакте с материнской кровью, и синцитиальный дебрис в виде узлов или ядерных агрегатов может быть обнаружен в материнской циркуляции с увеличением срока беременности [76, 77]. Постоянный кровоток к синцитиотрофобласту вызывает быстрые изменения старения и требует активации аутофагии для их удаления при неосложненной беременности [8, 78, 79].Во время преэклампсии синцитиотрофобласт испытывает ускоренное старение с активацией апоптотического каскада, некротическим распадом с высвобождением некротического мусора и увеличением синцитиальных агрегатов [77, 80]. Было замечено, что синцитиотрофобласт секретирует ассоциированную со старением бета-галактозидазу (SA β -Gal) вместе с повышением проапоптотических ингибиторов p53 и CDK, что указывает на прекращение клеточного цикла и старение [81, 82].
Недавний обзор Кокса и Редмана описывает биохимический путь и механизм старения плацентарных клеток после окислительного стресса [8].Они подчеркивают, что раннее начало старения при преэклампсии может быть связано с чрезмерным накоплением ROS и стрессом окислительного / эндоплазматического ретикулума (ER), что приводит к активации пути mTORC (регулятор клеточного цикла) и продукции белков секреторного фенотипа, ассоциированного со старением (SASP), которые затем активирует путь циклооксигеназы и усиливает выработку провоспалительных цитокинов и хемокинов [8].
4. Клеточное старение при неблагоприятных исходах беременности
Трофобласты имитируют раковые клетки, проявляя инвазивность, чтобы поддерживать рост плода.Подобно опухолевым клеткам, трофобласты сохраняют свою длину теломер и уровень обратной транскриптазы теломеразы человека (hTERT) при неосложненной беременности [83, 84]. В течение первого триместра трофобласт испытывает низкое давление кислорода или физиологическое гипоксическое состояние, связанное с активацией HIF-1 α . Это состояние низкого напряжения кислорода отвечает за моделирование архитектуры ворсинок и поддержание клеточной целостности за счет сохранения длины теломер и активации ферментов теломеразы [85, 86].Это физиологическое состояние изменяется в конце первого триместра, когда плацента насыщается кислородом [87]. Длина теломер остается постоянной на протяжении нормальной беременности, но в определенных условиях, таких как ограничение роста плода и неконтролируемый диабет, длина теломер значительно сокращается [88, 89]. Изменения теломер могут быть связаны с повышенным окислительным стрессом, что приводит к повреждению ДНК и активации ответа на повреждение (DDR) через путь p53 и способствует старению трофобласта [9, 84].В 2010 году Бирон-Шентал и др. были первыми, кто сообщил о доказательствах клеточного старения при преэклампсии и задержке роста плода. Они продемонстрировали, что при преэклампсии и беременностях с ЗВР теломеры значительно короче в трофобласте со сниженной экспрессией hTERT с повышенной частотой агрегатов теломер по сравнению с неосложненными беременностями [90]. Эти плацентарные изменения отсутствовали на сроках 37-41 недель беременности, что указывает на преждевременное старение плаценты при этих осложнениях беременности [90].
Плацента стареет постепенно, и присутствие маркеров старения, таких как белки p21, p16, p53 и Rb, приближающие к этому термину, поддерживает гипотезу старения нормальной плаценты [91]. Недавно в исследовании Nuzzo et al. показаны изменения клеточного цикла с усиленной регуляцией циклина D1 (регулятор клеточного цикла) и PARP1 (экспрессируемого на повреждении ДНК и возрастных изменениях) с понижающей регуляцией JunB (гена супрессора старения) в мезенхимальных стромальных клетках плаценты (PMSC), экстрагированных из преэкламптической плаценты, при сравнении к нормальной плаценте [92].Кроме того, Sharp et al. обнаружили дисбаланс между передачей сигналов p53 (индуцирующий старение и проапоптотический ген) и MDM2 (супрессор p53) в белках плаценты в синцитиотрофобласте, но не в цитотрофобласте у пациентов с преэклампсией с ранним началом [93]. Наконец, Gao et al. сообщили о повышении регуляции передачи сигналов p53 и остановке клеточного цикла с активацией проапоптотических BAX и белков каспазы в эндотелиальных клетках пупочной вены человека (HUVEC), взятых у пациентов с преэклампсией, по сравнению с контрольной группой неосложненной беременности [94].
Активация путей DDR, мутации мтДНК и эндогенный стресс, такой как накопление ROS и редокс-сигналы, могут вызывать эпигенетические модификации. Эпигенетику можно определить как физиологические изменения, которые нельзя отнести к генетическому коду, а скорее такие модификации, как фосфорилирование, ацетилирование или метилирование ДНК или гистоновых белков в ядре [95]. Либо эти изменения могут быть адаптивной реакцией на постоянные стимулы, либо они могут быть вирулентными модификациями, ведущими к необратимым изменениям в половых клетках [96].Связь между эпигенетикой, старением и возрастными расстройствами была продемонстрирована в нескольких исследованиях. Ремоделирование хроматина может включать метилирование или деметилирование гистоновых остатков в определенных сайтах, что может вызывать эпигенетические изменения внутри клеток [95, 96]. Lowe et al. В ходе своих исследований эндотелиальных клеток, собранных из коронарной артерии 19-летнего мужчины, обсуждали, что клеточное старение можно точно оценить с помощью внутренних свойств клеток, известных как эпигенетические часы, на которые указывает специфическое метилирование ДНК или цитозин. метилирование CpG-островков, которое при определенных условиях может ускорять старение [97].Madrigano et al. В своем продольном исследовании среди пожилых людей показали, что специфичное для генов метилирование ДНК тесно связано со старением и возрастными расстройствами [98].
Были продемонстрированы эпигенетические изменения в ткани плаценты, включая паттерны метилирования ДНК, связывающую способность ДНК-связывающих белков или DBP (особенно в гене цитохрома p450), паттерны метилирования импринтированных областей в генах h29 / IGF2 и метилирование гистоновых белков внутри гормон роста человека в плацентарном хроматине [99].В недавнем исследовании Eddy et al., Модификации гистонов были очевидны в трофобласте плаценты BeWo при воздействии гипоксических условий с выраженным гипометилированием цитозина, эпигенетическим изменением, обычно очевидным при возрастных патологиях [100].
5. Изменения старения, связанные с митохондриальной дисфункцией, в плаценте
Плацента — это орган с высоким уровнем метаболизма, требующий устойчивой митохондриальной активности. Даже при нормальной функции митохондрий постоянные изменения во вневорсинчатом трофобласте (EVT) и ремоделирование сосудов приводят к увеличению продукции АТФ за счет окислительного фосфорилирования [101, 102].
Накопление АФК, таких как супероксид, оксиды азота и пероксинитрит, приводит к окислительному стрессу на ранних сроках беременности [101]. АФК представляют собой сигнальные молекулы, которые преобладают над апоптотическими, окислительно-восстановительными и воспалительными сигнальными путями соответственно [103, 104]. АФК могут быть получены из ряда источников, включая митохондрии (mROS), НАДФН-оксидазы, ксантиноксидазу или фермент p450 [105, 106]. Активные формы кислорода (АФК) изменяют макромолекулы за счет окислительного повреждения белков, влияющих на функционирование генов, перекисного окисления липидов с усилением циркуляции полиненасыщенных жирных кислот и потери целостности клеточной мембраны [107–109].Повышенная регуляция АФК и ее побочных продуктов, отсутствие клиренса и редокс-сигнализация имеют прямые связи как с митохондриальным, так и с клеточным старением. В дополнение к этим изменениям окислительный стресс активирует путь митоген-активированной протеинкиназы (MAPK) через стресс-активированную протеинкиназу / Jun N-концевую киназу (SAPK / JNK) или путь p38 в ответ на повреждение ДНК, что в дальнейшем приводит к прекращение клеточной пролиферации и клеточного старения [110].
Было показано, что в пределах плаценты нитрование белка и перекисное окисление липидов значительно выше в тканях, выделенных от пациентов с преэклампсией, по сравнению с неосложненной беременностью [111–113].Перекисное окисление липидов может быть ферментативным, катализируемым ферментами липоксигеназы, или неферментативным в присутствии свободных радикалов [114]. Неферментативное перекисное окисление липидов активируется с возрастом, и его продукты сильно выражаются при возрастных заболеваниях, таких как атеросклероз [115]. В 1998 г. Wang и Walsh описали, что перекисное окисление липидов плаценты было значительно выше при преэклампсии [111]. Они установили, что высокие уровни перекисного окисления липидов являются результатом увеличения митохондриальной массы при плохом сосудистом кровотоке, необходимом для удовлетворения энергетических потребностей при преэклампсии [111].
Различные систематические обзоры указывают на повышенные уровни окисления липидов в преэклампсической сыворотке и плазме матери, что обычно связано с нарушением антиоксидантной защиты по сравнению с неосложненной беременностью [116, 117].
Низкая васкуляризация плаценты приводит к уменьшению размера, количества и активности митохондрий [118, 119]. Недавнее исследование Venkata et al. С использованием модели преэклампсии со сниженным давлением маточной перфузии (RUPP) у крыс показало значительное снижение митохондриального дыхания, особенно на стадии 3, и увеличение выработки перекиси водорода по сравнению с контрольными крысами [118].
Передача сигналов оксида азота регулирует клеточные процессы, такие как апоптоз, дифференцировка и деление [120]. На вневорсинчатую активность трофобластов, такую как миграция и инвазия, могут влиять два подтипа оксидов азота, eNOS (эндотелиальная синтаза оксида азота) и iNOS (индуцибельная синтаза оксида азота) [120]. Нитрование белков может либо не иметь эффекта, либо демонстрировать потерю / усиление функциональности. В плаценте пероксинитрит может изменять реактивность сосудов и маточно-плацентарное кровообращение при таких осложнениях беременности, как преэклампсия [91, 121].Повышение активности NOS и накопление пероксинитрита при преэклампсии может привести к подавлению митохондриальной активности за счет ингибирования цепи переноса электронов и нитрования митохондриальных белков и антиоксидантов, таких как митохондриальная супероксиддисмутаза (MnSOD), наряду с активацией трофобластного апоптоза [122].
Как показано на Рисунке 1, старение обычно связано с митохондриальной дисфункцией как прямым следствием потери митохондриальной динамики и увеличения митохондриального повреждения [122, 123].Митохондрии подвергаются непрерывному делению и слиянию для поддержания митохондриальной динамики, нарушение которой может привести к накоплению митохондриального мусора и ухудшению функционирования митохондрий [122, 123]. Считается, что митохондриальная динамика изменяется при преэклампсии с измененной экспрессией генов митохондриальных регуляторов аутофагии, таких как OPA1, SIRT3 и MNF2 / 1, но были проведены ограниченные исследования для полного понимания процесса передачи сигналов [124, 125]. Недавно Ausman et al. сообщили, что динамика митохондрий при преэклампсии склонна к делению митохондрий с повышенным фосфорилированием гена DERP1 в митохондриях, выделенных из преэклампсической плаценты [126].Эти изменения сопровождались накоплением церамидов, которые активировали BOK, проапоптотический белок в преэкламптических тканях плаценты по сравнению с нормальной плацентой, что указывает на усиление трофобластной аутофагии при преэклампсии и ЗВУР [126].
Антиоксиданты вырабатываются клетками для нейтрализации продуктов АФК, превращая их в кислород и перекись водорода, которая далее расщепляется с образованием воды. Антиоксиданты также считаются средствами против старения и могут быть разделены на подтипы: ферментативные, такие как супероксиддисмутазы (SOD), каталазы и пероксидазы, или неферментативные, такие как витамины (A, C и E), билирубин и мочевая кислота [127, 128 ].Окислительный стресс возникает, когда существует дисбаланс между побочными продуктами АФК, производимыми и улавливаемыми антиоксидантами [128, 129]. Все основные антиоксиданты локализуются в плаценте для снижения окислительного стресса, и их активность зависит от степени стресса, испытываемого клетками [71]. При преэклампсии и ЗВУР антиоксидантная активность ослаблена по сравнению с неосложненной беременностью, как показано на Рисунке 1 [127].
6. Маркеры старения при неблагоприятных исходах беременности
Основной акушерской проблемой было определение биомаркеров для выявления таких осложнений беременности, как преэклампсия и ЗВУР, в жидкостях организма матери.Различные маркеры митохондриальной дисфункции и окислительного стресса были исследованы как ранние биомаркеры нарушений беременности, как показано в таблице 1. В 2012 году Qiu et al. были первыми, кто сообщил о повышенных уровнях мтДНК в материнской периферической крови при преэклампсии, что указывает на высокий окислительный стресс и митохондриальную дисфункцию [132]. Недавнее исследование методом случай-контроль, проведенное Williamson, McCarthy и Kenny, обнаружило повышенное количество копий мтДНК в материнской плазме на 15-20 неделе беременности при преэклампсии по сравнению с таковыми при неосложненной контрольной беременности [133, 134].Кроме того, это исследование также продемонстрировало значительное снижение уровня антиоксидантной митохондриальной супероксиддисмутазы (mSOD) на 15 неделе беременности у женщин, у которых позже развилась преэклампсия, таким образом подтверждая митохондриальную дисфункцию как патофизиологическое событие при преэклампсии [134]. В другом аналогичном исследовании Marschalek et al. показали аналогичные результаты с повышенным числом копий мтДНК в материнской сыворотке, обнаруживаемым при преэклампсии с ранним началом [135].
| ||||||||||||||||||
Помимо митохондриальной дисфункции, воспаление и медиаторы воспаления проявляются в преждевременном старении плаценты.Некоторые ассоциированные со старением воспалительные маркеры, такие как секреторные фенотипы, ассоциированные со старением (SASP), повышены при преэклампсии [136].
Kupferminc et al. показали, что TNF- α значительно повышен в околоплодных водах и материнской плазме при тяжелой преэклампсии [137]. sST2 (растворимый ST2) является членом семейства интерлейкинов-1, в большом количестве экспрессируется в эндотелиальных клетках и обычно связан с возрастными расстройствами, такими как сердечные заболевания [138]. В случае повышенной гибели клеток и некротической передачи сигналов путь IL33 / STL2 запускается активацией Toll-Like Receptor-1 (TLR1), что приводит к усилению регуляции притока цитокинов и хемокинов [139].Недавнее лонгитюдное исследование Romero et al. сообщили о значительном повышении уровня sST2 в материнской плазме у пациентов из группы риска почти за 6 недель до развития преэклампсии [140].
МикроРНК (miRNA) и длинные некодирующие РНК (lncRNA) представляют собой некодирующие РНК, которые обладают потенциалом для регуляции генов [141]. miRNA доступны в жидкостях организма и в настоящее время регулярно исследуются как биомаркеры, так и в качестве перспективных терапевтических средств. В матке miRNA контролируются стероидными гормонами и отвечают за эффективную плаценту.Недавняя работа Tan et al. заявили, что в неблагоприятных условиях плаценты, таких как преэклампсия, длинная некодирующая РНК, lncRNA DLX6-AS1, сверхэкспрессируется в линиях трофобластных клеток, что приводит к усилению регуляции mir-376c, который отвечает за остановку клеточного цикла [142].
7. Возможные терапевтические средства и перспективы развития неблагоприятных исходов беременности
Старение — это однонаправленный процесс, который нельзя обратить вспять; однако исследования, направленные на снижение окислительного стресса за счет восстановления митохондриальной пригодности, могут быть потенциальной терапией неблагоприятных исходов беременности [143].Пригодность митохондрий признана ключевым регулятором развития клеточного цикла и метаболизма с митохондриальными взаимодействиями с другими органеллами, включая ядро и эндоплазматический ретикулум (ER), обеспечивая гомеостаз клеточной динамики и жизнеспособности. При осложнениях беременности хронический окислительный стресс приводит к дисфункции митохондрий, что приводит к потере стабильности митохондриальной передачи сигналов [102]. Антиоксидантные добавки, такие как витамины C и E, принимаемые во время беременности, не продемонстрировали каких-либо значительных эффектов в снижении окислительного стресса.
Однако продолжающиеся исследования более эффективных антиоксидантов пролили свет на несколько цитопротективных агентов, нацеленных на митохондрии.
Недавнее исследование продемонстрировало, что митохондрии, нацеленные на антиоксидант, MitoTEMPO, обладают цитопротектором против гибели клеток, индуцированной АФК [134]. Когда клетки HUVEC были предварительно обработаны MitoTEMPO перед воздействием 3% плазмы беременных с преэклампсией, это привело к значительному снижению выработки клеточного супероксида, нормализации функционирования митохондрий и снижению воспалительного притока [134].Недавно другое исследование, проведенное Nuzzo et al. демонстрирует, что у беременных крыс, нацеленных на митохондриальный антиоксидант MitoQ, наблюдается нормализованный объем плаценты и устранена задержка роста плода в условиях гипоксии [144]. Кроме того, они обсудили, что MitoQ обладает потенциалом для регулирования клеточного цикла посредством пути передачи сигналов пролиферации MAPK [144].
Наконец, эрготионеин — это водорастворимая аминокислота, обладающая цитопротекторным действием. Эрготионеин в первую очередь нацелен на митохондрии и может улавливать АФК, индуцировать клеточную пролиферацию и репарацию посредством активированных антиоксидантных путей [145].Множество преимуществ антиоксидантов, направленных и нормализующих функционирование и динамику митохондрий, могут стать потенциальными пренатальными терапевтическими средствами для лечения неблагоприятных исходов беременности [145].
8. Заключение
Старение полезно для многоклеточных организмов, особенно для устранения мутаций и предотвращения рака. Однако при наличии стойкого нежелательного стресса этот процесс может неестественно ускориться и привести к серьезным осложнениям для здоровья. При неблагоприятных исходах беременности, таких как преэклампсия и ограничение роста плода, плацентарная недостаточность сопровождается аберрантной сигнализацией преждевременного старения плаценты и апоптоза.Как показано на Рисунке 1, в этом обзоре освещены текущие знания о роли митохондриальной дисфункции плаценты, клеточного старения и оси старения плаценты в неблагоприятных исходах беременности.
Дальнейшие исследования должны быть сосредоточены на углублении нашего понимания преждевременного старения плаценты как патофизиологии нарушений беременности и изучении новых способов улучшения результатов, таких как преэклампсия и ограничение роста плода.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Вклад авторов
Катал Маккарти и Фергус П. Маккарти внесли одинаковый вклад.
Благодарности
Этот проект финансируется программой исследований и инноваций Европейского Союза Horizon 2020 в рамках сети инновационного обучения действий Марии Склодовской-Кюри (h3020-MSCA-ITN 2017), грант № 765274, аббревиатура iPLACENTA (http: // www. .iplacenta.eu).
Преждевременное старение плаценты из-за окислительного стресса — ScienceDaily
Новое исследование, проведенное учеными из Медицинского отделения Техасского университета в Галвестоне, впервые показало, что преждевременное старение плаценты из-за окислительного стресса является причиной многих преждевременных родов. .Исследование опубликовано сегодня в Американском журнале патологии.
Исследователи взяли плодные оболочки, подвергли их окислительному стрессу в лабораторных условиях (в частности, экстракт сигаретного дыма) и изучили, вызывает ли он быстрое старение плацентарной ткани. Это было так.
Факторы окислительного стресса включают токсины и загрязнение окружающей среды и являются неизбежным компонентом нормальной жизни. Однако других факторов, таких как курение и употребление алкоголя, высокий индекс массы тела, плохое питание и инфекции, можно было бы избежать.
Антиоксиданты в организме контролируют любые повреждения, вызванные окислительным стрессом. Но когда оксидативный стресс становится непреодолимым, он может вызвать преждевременное старение плаценты, что может привести к преждевременным родам.
По словам исследователей, антиоксидантные добавки во время беременности не смогли снизить количество преждевременных родов, потому что механизмы повреждения, вызываемого окислительным стрессом, все еще не ясны.
«Это первое исследование, в котором изучается и доказывается, что окислительный стресс вызывает старение или старение в эмбриональных клетках человека», — сказал д-р.Рамкумар Менон, доцент кафедры акушерства и гинекологии UTMB и ведущий исследователь исследования. «С более чем 15 миллионами беременностей во всем мире, заканчивающихся преждевременными родами, теперь мы можем двигаться вперед в изучении того, как эта информация может привести к более совершенным стратегиям вмешательства для снижения риска преждевременных родов».
Предыдущие исследования показали, что инфекция является основной причиной преждевременного разрыва плодных оболочек (pPROM, или разрыв мешка с водой во время беременности), при котором антибиотики являются стандартным вмешательством.
Однако исследователи UTMB обнаружили, что такие меры, как применение антибиотиков и антиоксидантов, не помогли предотвратить преждевременные роды. «Это исследование предоставляет доказательства того, что существуют и другие факторы, на которые медицинское сообщество должно обратить внимание, когда они вызывают спонтанные роды», — сказал Менон.
Исследование является частью продолжающихся усилий по лучшему пониманию pPROM или самопроизвольных родов до 37 недель беременности и было поддержано фондами развития Отделения акушерства и гинекологии UTMB.
История Источник:
Материалы предоставлены Медицинским отделением Техасского университета в Галвестоне . Примечание. Содержимое можно редактировать по стилю и длине.
Старение плаценты | ADC Fetal & Neonatal Edition
Широко распространено мнение, что в течение относительно короткого периода нормальной беременности плацента постепенно стареет и, в конце концов, находится на грани морфологического и физиологического старения.1-3 Это убеждение основано на очевидном совпадении клинических, структурных и функциональных данных, все из которых были восприняты, довольно некритически, как поддерживающие эту концепцию плаценты как стареющего органа, причем слишком часто без каких-либо различий между ними. между изменениями, связанными со временем, и настоящими изменениями старения. Я рассмотрю некоторые из этих концепций и рассмотрю, действительно ли плацента претерпевает процесс старения. Для целей этого обзора старение считается внутренним, пагубным и прогрессирующим изменением, которое приводит к необратимой потере функциональной способности, нарушению способности поддерживать гомеостаз и снижению способности восстанавливать повреждения.
Морфологические изменения
Плацента необычна тем, что ее основная гистологическая структура претерпевает значительные изменения на протяжении всей жизни. В течение некоторого времени было принято описывать внешний вид ворсинок плаценты с точки зрения их изменения внешнего вида по мере прогрессирования беременности, сравнивая, например, типичные ворсинки первого триместра с ворсинками в плаценте третьего триместра. Часто подразумевается, что это изменение внешнего вида является процессом старения, но теперь признано, что эта временная изменчивость во внешнем виде ворсинок отражает постоянное развитие и ветвление ворсинчатого дерева (рис.1). ворсинчатое дерево и гистологический внешний вид ворсинок были формально кодифицированы5-8 с идентификацией пяти типов ворсинок (рис. 2).
Рисунок 1Схематическое изображение периферического ворсинчатого дерева, показывающее большую центральную ворсинку стебля: боковые ветви от этого являются зрелыми промежуточными ворсинками, из которых выступают терминальные ворсинки.
фигура 2Изображение периферических ветвей зрелого ворсинчатого дерева вместе с типичными поперечными сечениями пяти типов ворсинок. Рисунки воспроизводятся из Haines & Taylor. Учебник акушерской и гинекологической патологии. 4-е изд. 1995 г., с любезного разрешения Черчилля Ливингстона и профессора П. Кауфмана.
1
Мезенхимальные ворсинкиОни представляют собой преходящую стадию развития плаценты и могут дифференцироваться как на зрелые, так и на незрелые промежуточные ворсинки. Они составляют первое поколение новообразованных ворсинок и происходят из ростков трофобласта путем мезенхимальной инвазии и васкуляризации. Они обнаруживаются в основном на ранних стадиях беременности, но некоторые из них могут быть обнаружены и в срок.Они имеют полную трофобластическую оболочку с множеством цитотрофобластных клеток и регулярно рассредоточенными ядрами в синцитиотрофобласте: их рыхлая, незрелая строма обильна и содержит несколько гобауэровских клеток. клетки вместе с плохо развитыми капиллярами плода.
2
Незрелые промежуточные ворсинкиЭто периферические отростки стволовых ворсинок, которые являются преобладающей формой, наблюдаемой у незрелой плаценты. Эти ворсинки имеют хорошо сохранившуюся трофобластическую мантию, в которой много цитотрофобластических клеток; синцитиальные ядра распределены равномерно, синцитиальных узлов или васкулосинцитиальных мембран нет. У них имеется обильная рыхлая строма, которая содержит множество клеток Хофбауэра: присутствуют капилляры, артериолы и венулы.
3
Стеблевые ворсинкиСюда входят основные стебли, которые соединяют ворсинчатое дерево с хорионической пластиной, до четырех поколений коротких толстых ветвей и последующие поколения дихотомических ветвей. Их основная роль заключается в том, чтобы служить опорой для периферического ворсинчатого дерева, и до одной трети общего объема ворсинок зрелой плаценты составляют ворсинки этого типа, причем доля таких ворсинок наиболее высока в центральной части. субхориальная часть ворсинчатого дерева.Гистологически стволовые ворсинки имеют компактную строму и содержат либо артерии и вены, либо артериолы и венулы; также могут присутствовать поверхностно расположенные капилляры.
4
Зрелые промежуточные ворсинкиЭто периферические ответвления стеблей ворсинок, из которых непосредственно возникает большинство терминальных ворсинок. Они большие (60–150 мкм в диаметре) и содержат капилляры, смешанные с мелкими артериолами и венулами, причем сосуды расположены в очень рыхлой строме, занимающей более половины объема ворсинок.Синцитиотрофобласт имеет однородную структуру, без узлов или васкулосинцитиальных мембран. До четверти ворсинок зрелой плаценты относятся к этому типу.
5
Концевые ворсинкиЭто последние ответвления ворсинчатого дерева, похожие на виноградные выросты из зрелых промежуточных ворсинок. Они содержат капилляры, многие из которых синусоидально расширены и занимают большую часть диаметра поперечного сечения ворсинки. Синцитиотрофобласт тонкий, а синцитиальные ядра распределены неравномерно.Могут присутствовать синцитиальные узлы и обычно видны васкулосинцитиальные мембраны. Эти терминальные ворсинки начинают появляться примерно на 27-й неделе беременности и составляют 30-40 процентов объема ворсинок, 50 процентов площади поверхности ворсинок и 60 процентов ворсинок, видимых в поперечном сечении в срок.
Таким образом, ворсинчатое дерево развивается следующим образом: в первые недели беременности все ворсинки мезенхимального типа. Между 7-й и 8-й неделями мезенхимные ворсинки начинают трансформироваться в незрелые промежуточные ворсинки, которые впоследствии превращаются в стволовые ворсинки.Развитие дополнительных незрелых промежуточных ворсинок из мезенхимальных ворсинок постепенно прекращается в конце второго триместра, но эти незрелые промежуточные ворсинки продолжают созревать в стволовые ворсинки, и лишь некоторые из них остаются зонами роста в центрах долек. В начале третьего триместра мезенхимальные ворсинки перестают превращаться в незрелые промежуточные ворсинки и начинают трансформироваться в зрелые промежуточные ворсинки. Последние служат каркасом для терминальных ворсинок, которые начинают появляться вскоре после этого и преобладают в срок.
Это прогрессивное развитие ворсинчатого дерева приводит к преобладанию терминальных ворсинок в зрелой плаценте. Такие ворсинки условно классифицируются как «ворсинки третьего триместра», и сравнение их структуры с преобладающим типом ворсинок в первом триместре — незрелыми промежуточными ворсинками — привело многих к предположению, что по мере прогрессирования беременности ворсинчатый трофобласт становится нерегулярно истонченным и цитотрофобласт регрессирует, изменения интерпретируются как имеющие возрастную природу.Ворсинчатый цитотрофобласт, который является стволовой клеткой для трофобласта, в действительности не регрессирует, потому что абсолютное количество этих клеток в плаценте не уменьшается в срок, а фактически продолжает увеличиваться на протяжении всей беременности. Кажущаяся редкость этих клеток объясняется их более широкой дисперсией в значительно увеличенной общей массе плаценты. 10 Очаговое истончение синцитиотрофобласта ворсинок, обнаруживаемое во многих терминальных ворсинках, часто упоминалось как свидетельство синцитиального старения.Эти истонченные области на самом деле представляют собой «васкулосинцитиальные мембраны» 11, которые, хотя и образованы частично путем механического растяжения трофобласта за счет раздувания капиллярных петель 12, тем не менее ферментативно и ультраструктурно отличаются от немембранозных участков синцития. и являются областями синцитиотрофобласта, специфически дифференцированными для облегчения переноса газа.13 Таким образом, эти мембраны являются проявлением топографической функциональной дифференциации внутри трофобласта.
Взаимосвязанные, но отдельные процессы созревания ворсинчатого дерева и функциональной дифференциации трофобласта приводят к преобладанию ворсинчатой формы, оптимально адаптированной для механизмов диффузии материнско-плодного переноса: морфологические изменения существенно увеличивают площадь трофобластической поверхности14 и значительно сокращают гармоническое среднее расстояние диффузии между кровью матери и плода 15, что приводит к увеличению проводимости диффузии кислорода.16
Различать созревание, которое приводит к повышению функциональной эффективности, от старения, которое приводит к снижению функциональной эффективности, — это не просто педантизм. В этом отношении стоит отметить, что часть плаценты от женщин с тяжелой преэклампсией выглядят необычно зрелыми для продолжительности периода беременности: это обычно классифицируется как «преждевременное старение», но было бы правильнее учитывать изменения. поскольку это происходит из-за ускоренного созревания, это является компенсаторным механизмом для увеличения способности плаценты к переносу в условиях неблагоприятной материнской среды.
Следует признать, что механизмы контроля созревания плаценты неизвестны. Есть много агентов, которые считаются важными для контроля роста плаценты, включая цитокины, факторы роста, онкогены, простагландины и лейкотриены, 17-20, но далеко не ясно, можно ли приравнять контроль роста к контролю созревания. Однако развитие ворсинок, особенно на поздних стадиях беременности, по-видимому, в основном обусловлено пролиферацией эндотелиальных клеток и ростом капилляров.21 Факторы роста эндотелия сосудов присутствуют в ткани плаценты22, и предположение о том, что гипоксия может стимулировать ангиогенез, 23 и, таким образом, играть важную роль в развитии плаценты, подтверждает ускоренное созревание плаценты, наблюдаемое в некоторых случаях материнской преэклампсии.
Рост плаценты
Долгое время считалось, что рост плаценты и синтез ДНК прекращаются примерно на 36-й неделе беременности и что любое последующее увеличение размера плаценты происходит скорее из-за увеличения размера клеток, чем из-за увеличения числа клеток.24 Простое гистологическое исследование термина «плацента», однако, поможет опровергнуть эту точку зрения, поскольку незрелые промежуточные ворсинки часто присутствуют в центрах долек, и они явно представляют собой зону постоянного роста. Более того, общее содержание плацентарной ДНК продолжает увеличиваться почти линейно до 42-й недели беременности и после нее.25 Этот результат согласуется с авторадиографическими исследованиями и исследованиями проточной цитометрии, которые показали продолжающийся синтез ДНК в терминах «орган» 26-28 и с морфометрическими данными. исследования, которые показали стойкий рост ворсинок, продолжающееся расширение площади поверхности ворсинок и прогрессирующее ветвление ворсинчатого дерева до и после срока.14 29
Рост плаценты, безусловно, замедляется, но явно не прекращается в течение последних нескольких недель беременности, хотя это снижение скорости роста не является ни неизменным, ни необратимым, потому что плацента может продолжать увеличиваться в размерах, если столкнется с неблагоприятной материнской средой, такой как как беременность на большой высоте или тяжелая материнская анемия, в то время как возможность возобновления роста демонстрируется пролиферативным ответом на ишемическое синцитиальное повреждение. Те, кто утверждает, что снижение скорости роста плаценты на поздних сроках беременности является свидетельством старения, часто сравнивают плаценту с таким органом, как кишечник, в котором постоянная жизнеспособность зависит от постоянно реплицирующегося слоя стволовых клеток, производящего короткоживущие постмитотические клетки.Более подходящим было бы сравнение с таким органом, как печень, которая образована в основном из долгоживущих постмитотических клеток и который после достижения оптимального размера для удовлетворения возлагаемых на него метаболических требований не показывает мало доказательств клеточной пролиферации, в то время как сохраняя скрытую способность к активности роста. Кажется, нет веских причин, по которым плацента, когда она достигла размера, достаточного для адекватного выполнения своей передаточной функции, должна продолжать расти, и термин «плацента» с ее значительной функциональной резервной способностью более чем соответствует этой цели.
Функциональная активность
Было проведено несколько вертикальных исследований функции плаценты на протяжении всей беременности, но нет никаких доказательств того, что какие-либо из основных показателей снижения функции плаценты, а именно, пролиферативной, транспортной и секреторной способности.30 Как уже отмечалось, диффузионная проводимость органа увеличивается, в основном, в результате морфологических изменений, но есть значительные доказательства того, что специфические системы переноса, опосредованные плацентарным носителем, также увеличиваются.20 Плацентарное производство гормонов не ослабевает до наступления срока беременности: синтез хорионического гонадотропина человека снижается к концу первого триместра, но это явно связано с переключением генов, которое приводит к прогрессивному увеличению секреции плацентарного лактогена человека.
Плацента также сохраняет свою полную пролиферативную способность до срока, о чем свидетельствует ее способность восстанавливать и заменять в результате пролиферации в цитотрофобластических клетках ворсинок синцитиотрофобласт ворсинок, который был ишемически поврежден у женщин с тяжелой преэклампсией.13
Клинические факторы
Единственным наиболее важным фактором, приводящим к убеждению в старении плаценты, является явно повышенная заболеваемость и смертность плода, связанные с длительной беременностью, что традиционно приписывается «плацентарной недостаточности», являющейся следствием старения органа1. 31 Раньше считалось, что около 11% беременностей продлеваются до 42-й недели гестации или дольше 32. 33: введение рутинного ультразвукового исследования на ранних сроках беременности снизило частоту длительных беременностей примерно до 6% 34, и даже было заявлено, что при очень точных исследованиях датирования частота действительно длительных беременностей не превышает 1%.35 Это ставит под сомнение достоверность значительной части исторической информации о рисках и неблагоприятных последствиях продолжительной беременности, но тем не менее широко признается, что перинатальная смертность увеличивается после 42-й недели гестации36.
Любое увеличение перинатальной смертности после 42-й недели беременности частично связано с высокой частотой развития макросомии плода: 10% новорожденных от продолжительной беременности весят более 4000 г и 1% — более 4500 г, и эти плоды подвергаются особому риску. осложнений, таких как дистоция плеча.Присутствие этого большого числа макросомных плодов является четким признаком того, что, по крайней мере, в этой подгруппе плацента продолжает функционировать и после 40-й недели беременности и остается способной поддерживать беспрепятственный рост плода.
Классический клинический синдром «недоношенного» младенца1 31 не часто встречается сегодня, но, кажется, явно связан с развитием маловодия. Нет сомнений в том, что объем околоплодных вод имеет тенденцию к уменьшению при продолжительной беременности39 и что маловодие связано с высокой частотой замедления сердечного ритма плода.36 Некоторые приписывают это сжатию пуповины, 40 41 но одно исследование, подтвердившее, что компрессия пуповины является обычным явлением при длительной беременности, не смогло связать такое сжатие с ацидозом плода. 42 Часто предполагается, и действительно обычно утверждается, что уменьшение объема околоплодных вод в этих случаях является показателем о «плацентарной недостаточности», но на самом деле нет никаких доказательств того, что на поздних сроках беременности плацента играет какую-либо роль в производстве околоплодных вод или в контроле объема околоплодных вод.43 год
Таким образом, две наиболее серьезные причины повышенной заболеваемости при длительной беременности явно не связаны с каким-либо изменением функциональной способности плаценты. Исследование плаценты от длительной беременности не показывает никаких доказательств увеличения частоты грубых аномалий плаценты, таких как инфаркты, кальцификация или массивное отложение фибрина в перивилле. Наиболее характерной гистологической аномалией, обнаруживаемой в некоторых случаях, но не во всех, является снижение перфузии плода через ворсинки плаценты.13 Сосуды ворсинок плода в норме в плаценте от длительной беременности44, и исследования допплеровской скорости потока, в целом, но не единодушно, показали, что в таких плацентах нет повышенного сосудистого сопротивления плода.45-47 Следовательно, снижение перфузии плода, вероятно, является следствием маловодие, потому что исследования кровотока в пупочной вене показали, что кровоток плода к плаценте часто снижается в случаях маловодия (48).
Следует признать, что патофизиология длительной беременности до конца не выяснена.Однако кажется совершенно очевидным, что любые побочные эффекты, которые могут возникнуть у плода при длительных сроках беременности, не могут быть связаны с плацентарной недостаточностью или старением.
Выводы
Обзор имеющихся данных показывает, что плацента не претерпевает истинных изменений старения во время беременности. На самом деле нет никаких логических оснований полагать, что плацента, которая является органом плода, должна стареть, в то время как другие органы плода не стареют: ситуация, при которой отдельный орган стареет в организме, который не стареет, является той, которая не встречаются ни в одной биологической системе.Устойчивая вера в старение плаценты была основана на путанице между морфологическим созреванием и дифференцировкой и старением, неспособности оценить функциональные ресурсы органа и некритическом принятии слишком поверхностной концепции «плацентарной недостаточности» как причины повышенной перинатальная смертность.
Миф о старении плаценты
Я доула и воспитатель по родовспоможению.
У меня также есть докторская степень в области физиологии репродукции и 20-летний опыт исследований, и я должен признаться: я ДЕЙСТВИТЕЛЬНО злюсь, когда женщинам предоставляют доказательства низкого качества (или вообще не предоставляют доказательств) в поддержку рекомендации по стимулированию труд.
Ношу ли я шляпу доула или шляпу ученого, я должен признать, что мне действительно надоела растущая эпидемия индукции родов по сомнительным причинам. В этой статье мы исследуем одну из наиболее распространенных причин индукции родов в срок: идея о том, что роды следует вызывать до достижения определенного срока беременности, потому что «более старая» плацента не так эффективна.
Я хочу прояснить одну вещь, прежде чем мы начнем: я НЕ выступаю против индукции, когда это оправдано убедительными медицинскими доказательствами и когда женщина взвешивает доказательства и решает, что риск продолжения беременности выше, чем риск индукции родов. (как, например, преэклампсия или уменьшение шевелений плода, или когда у женщины есть психологические причины, по которым она выбирает стимуляцию).
За последние 8 лет, в промежутках между занятиями по дородовой помощи и оказанием помощи женщинам, я слышал и был свидетелем сотен историй индукции, большинство из которых в конечном итоге было травмирующим для матери.
В моей сфере работы мы часто называем это «автокатастрофой», что звучит примерно так: 3 дня введения простагландина (часто вызывают больший стресс, потому что женщина не может находиться со своей семьей большую часть времени), затем через 24 часа синтоцинона и кесарева сечения в конце либо из-за дистресса плода, либо из-за «неспособности к прогрессу» (если бы только женщинам сказали: нам очень жаль, нам не удалось вызвать у вас роды с помощью наших препаратов, так что теперь единственный вариант — кесарево сечение, возможно, женщины не будут чувствовать такую травму, как когда их называют неудачником.Язык имеет значение).
Я слушал и поддерживал женщин (и их партнеров), когда они рассказывали мне о своем расстройстве, своем горе, своем неверии, отсутствии подготовки и своих чувствах неудач.
Одна из наиболее часто цитируемых причин побуждения женщин к беременности, превышающей 41 неделю, — это идея о том, что плацента каким-то образом перестает работать после того, как беременность достигает определенного количества недель.
Подразумевается, что у плаценты есть срок продажи, как у куска мяса в супермаркете.
Недавно было опубликовано еще больше статей, в которых утверждается, что плаценты «стареют», «разлагаются» и «выходят из строя» у матерей более старшего возраста и после определенного количества недель беременности.
В наши дни я обычно не люблю писать только о науке. Мне нравится писать о том, как я отношусь к проблемам, и вставлять несколько ссылок для людей, которые хотят их прочитать. Я провел 20 лет, занимаясь научными исследованиями в академической и промышленной среде. Я отошел от этого, я нахожу большую часть научного мира слишком сухим и, откровенно говоря, слишком ограниченным.
Но я теряю терпение из-за этой так называемой науки, причиняющей так много вреда женщинам.
Несколько недель назад я был очень обеспокоен, наблюдая за жаркими дебатами на эту тему в социальных сетях; видя, как многие из моих коллег вдыхаются, заставляя поверить в так называемую науку людьми, которые заявляют, что знают ответы на все вопросы, используя жаргон, которого они не понимают.
Я считаю, что мой научный опыт в сочетании с опытом работы тренером по дородовой помощи и доулой дает мне уникальный, широкий взгляд на эту тему.
Итак, пришло время снова надеть свою научную шляпу, проанализировать рассматриваемые статьи и предложить свою довольно альтернативную интерпретацию текущих данных, чтобы женщины и работники родовспоможения могли принимать действительно обоснованные решения, а не односторонние, основанные на мнениях. нескольких так называемых экспертов, чьи взгляды основаны на их существующих убеждениях и мнениях, а не на взвешенной оценке доказательств в этой области.
Предлагаю вам выпить чашку чая, потому что это будет долгое время!
Прежде чем я начну, я хочу отметить важное замечание: даже эксперты в какой-либо области часто не соглашаются друг с другом.
Когда я работал в академической сфере во время получения степени доктора философии и двух постдоков, работая в небольшой нишевой области биологических исследований (гены часов, гены, которые контролируют ритмы, такие как бодрствование и сон), я публиковал научные статьи с довольно высоким рейтингом. , и быстро стал признанным экспертом в своей области. Это привело к тому, что меня стали приглашать в качестве приглашенного докладчика на конференции. Я помню, как спорил до посинения по поводу интерпретации определенных данных с другими экспертами в этой области.Это было сделано страстно, но весело, с юмором и весельем. Это произошло потому, что, как я объясню ниже, хорошие ученые понимают, что наука — это не черное и белое.
Я вижу в социальных сетях не такие разговоры об этом исследовании. Я вижу экспертов, которые притворяются, что знают ответы на все вопросы, представляются единственными, у кого есть все знания, и откровенно обманывают и запугивают неученых с помощью жаргона.
В данном конкретном случае они занимают высокие моральные позиции, представляя себя спасителями, как будто мертворождение можно было бы предотвратить, если бы только мы вынуждали всех женщин на определенном количестве недель беременности.Они нападают на других людей, чьи взгляды отличаются, даже если эти люди имеют такую же или более высокую квалификацию и имеют докторскую степень в соответствующих областях.
Это неправильно. Это вредит женщинам, и это вредит людям, которые их поддерживают.
Даже в науке вещи никогда не бывают черно-белыми. Ничего не гарантировано. Есть много оттенков серого. И притворяться, что все обстоит таким образом, — это не наука, это заблуждение, и это относится к науке как к догме. Если вы хотите узнать больше об этом образе мышления, посмотрите запрещенную лекцию на эту тему кембриджского ученого доктора Руперта Шелдрейка на TED.
А теперь вернемся к теме: действительно ли плаценты стареют? Они перестают правильно функционировать к концу беременности? И самое главное, несут ли они единоличную ответственность за (давайте вспомним, крошечное) увеличение количества мертворожденных к концу беременности? Это предположения, которые в настоящее время лежат в основе нашей политики введения в должность.
Я чувствую, что сначала нужно объяснить, что риск увеличения числа мертворождений в срок, который является основной причиной политики индукции, на самом деле очень мал и возрастает примерно с 0.1% (1 из 1000) в 40-41 неделю, примерно до 0,3% (3 из 1000) в 42 недели и примерно 0,5% (5 из 1000) в 43 недели (из этой статьи). Кокрановский обзор индукции после истечения срока показал, что индукция до 42 недель снижает риск перинатальной смерти с 0,3% до 0,03%, и что авторы обзора пришли к выводу, что:
”Политика индукции родов по сравнению с выжидательной тактикой связана с меньшим количеством перинатальных смертей и меньшим количеством кесарева сечения. Некоторые младенческие заболевания, такие как синдром аспирации мекония, также были уменьшены с помощью политики индукции послеродовых родов, хотя не было замечено значительных различий в частоте поступления в ОИТН.Однако, абсолютный риск перинатальной смерти невелик. Женщин следует соответствующим образом проконсультировать, чтобы сделать осознанный выбор между плановой индукцией при послеродовой беременности или мониторингом без индукции (или отсроченной индукции) ».
На практике я почти никогда не вижу, чтобы часть, выделенная жирным шрифтом, была представлена как вариант для женщин (читайте об этом в моем предыдущем блоге здесь)
Я хотел бы процитировать основополагающую статью покойного доктора Фокса «Старение плаценты»
”Обзор имеющихся данных показывает, что плацента не претерпевает истинных изменений старения во время беременности. На самом деле нет никаких логических оснований полагать, что плацента, которая является органом плода, должна стареть, в то время как другие органы плода нет: ситуация, при которой отдельный орган стареет в организме, который не стареет, является той, которая не встречается ни в одной биологической системе. Устойчивая вера в старение плаценты была основана на путанице между морфологическим созреванием и дифференцировкой и старением, неспособности оценить функциональные ресурсы органа, и некритическом принятии слишком поверхностной концепции «плацентарной недостаточности» как причины повышенной перинатальной смертности .”
Хотя я полностью осознаю, что эта статья датирована 1997 годом, и что с тех пор было проведено гораздо больше исследований, я все еще верю, что его вывод остается в силе, особенно последнее предложение.
Я слышал, как многие медицинские работники принуждают будущих мам принять индукцию (помните, если вы чувствуете принуждение, это не согласие) на крики «ваша плацента сейчас не работает». Однако даже сегодня мы не знаем, чем объясняется крошечный рост неонатальной смертности через 40 недель.
Похоже, существует сильное желание доказать причинную связь между старением плаценты и увеличением числа мертворожденных, и это желание руководствуется позитивным стремлением к сокращению числа мертворождений.
Я сочувствую этому побуждению больше, чем вы думаете, потому что мой младший брат был мертворожденным, поэтому я полностью понимаю разрушительные последствия смерти новорожденного для семьи.
Но пока это всего лишь теория.
И любой может выдумать теорию о чем угодно, но это не соответствует действительности.
Нам нужно найти баланс между реальной статистикой и желаниями женщин о положительных впечатлениях от родов. Поскольку данные в этой области не оставляют сомнений в том, что, пока мать и ребенок здоровы, для всех участников лучше начать роды самостоятельно.
Потому что мы не должны забывать, что индукции могут быть очень травматичными для женщин и могут вызвать дистресс у плода.
На самом деле все очень просто: пусть матери сами решают, чего они хотят.А для этого им нужны реальные факты и цифры, а не эмоциональное принуждение.
Сначала немного истории
Как вообще возникла концепция плацентарной недостаточности?
В своей книге «Стимулирование родов, принятие обоснованных решений» доктор Сара Уикхэм объясняет, что эта теория возникла сначала благодаря работе Баллантайна, описавшего истощение новорожденного в 1902 году, а затем Рунге в 1958 году, который ввел термин «плацентарная недостаточность» . Это стало известно как синдром Баллантайна-Рунге и привело к предположению о связи между продолжительностью беременности и плацентарной недостаточностью.
Доктор Уикхэм продолжает объяснять, что эта теория никогда не была доказана и что за ней нет никаких доказательств. Она объясняет, что, хотя мы знаем, что плаценты некоторых женщин иногда не обеспечивают достаточного количества питательных веществ для их ребенка, это не означает, что плаценты всех женщин обычно выходят из строя в определенный момент времени. Еще одно свидетельство того, насколько сильно те, кто оспаривает эту теорию, действительно заботится о благополучии младенцев, можно увидеть там, где доктор Уикхэм отмечает в своих выступлениях, что проблема заключается не только в предотвращении ненужных индукций для женщин, которые в них не нуждаются.Пытаясь дать стандартизованные рекомендации на уровне населения (или подход «один размер для всех»), мы не только приводим многих женщин к индукции, в которой они не нуждаются, но и можем не выявить и помочь небольшому количеству женщин. младенцы, которые действительно нуждаются в помощи, но в момент, предшествующий нынешнему пороговому значению для индукции на уровне популяции.
Даже в документах, утверждающих, что существует связь между продолжительностью беременности и состоянием плаценты, когда вы копаетесь в них, всегда приходит к выводу, что существует «возможная связь», а не доказанная.
И, как я объяснял ранее, эксперты в этой области не согласны друг с другом. В своей книге «Почему индукция имеет значение» доктор Рэйчел Рид цитирует несколько известных работ, в частности, статью Маити и др. , в которой утверждается прямая связь между старением плаценты и мертворождением, а также статью Мацзурато и др. ». Руководство по ведению беременных после родов », в котором говорится, что:
” Хотя риски для плода, матери и новорожденного увеличиваются после 41 недели, нет убедительных доказательств того, что продление беременности само по себе является основным фактором риска.Выявлены и другие специфические факторы риска неблагоприятных исходов, наиболее важными из которых являются задержка роста плода и пороки развития плода. Чтобы предотвратить PT (послеродовой) и сопутствующие осложнения, была предложена плановая индукция до 42 недель. Нет убедительных доказательств того, что эта политика улучшает исходы для плода, матери и новорожденного по сравнению с выжидательной тактикой ».
Суть аргументов в пользу теории старения плаценты
Некоторые из технических терминов, которые я часто встречаю, и которые вводят в заблуждение многих моих коллег, потому что не понимают их значения, — это морфологические изменения плаценты, такие как апоптоз, аутофагия, синцитиальные узлы, уменьшение длины теломер и т. .Во многих статьях авторы утверждают, что это ключевые особенности старения, наблюдаемые при послеродовом периоде плаценты.
Тем не менее, существует несколько интерпретаций этих морфологических изменений, которые так часто хвалят как доказательство плацентарного «срока годности». Они не означают автоматически наличие проблемы. Во многих отношениях наше понимание этой области находится в зачаточном состоянии, и нам лучше занять позицию научного смирения, пока мы пытаемся определить значение этих открытий.
Одним из наиболее ярких примеров исследования, в котором высказывается предположение, что старение плаценты в срок является свершившимся фактом, является это исследование с сенсационным названием: «Доказательства того, что смерть плода связана со старением плаценты», проведенное Maiti et al.
Я нахожу одно из высказываний в этой статье чрезвычайно тревожным:
”Известное экспоненциальное увеличение необъяснимой внутриутробной смерти, которое происходит на сроке> 38 недель беременности , может, таким образом, быть следствием старения плаценты и снижения способности адекватно удовлетворять возрастающие потребности растущего плода. Эти знания могут повлиять на акушерскую практику, чтобы гарантировать, что младенцы рождаются до того, как плацента дорастет до критической точки отказа “
Боюсь, что такое заявление будет использовано для давления на еще большее количество женщин, чтобы заставить их действовать раньше, не беспокоясь об их личном решении или благополучии. И все же, как я буду повторять, это все еще недоказанная теория, и разные эксперты по-разному относятся к тому, верна она или нет. Медицинская профессия основана на принципе «сначала не навреди», и я понимаю, что это означает, что мы не должны вмешиваться, если у нас нет веских доказательств, подтверждающих это.
Я проясню дифференциальную интерпретацию некоторых изменений, наблюдаемых в плаценте.
Одно из изменений, которые они наблюдают в этой статье, — снижение аутофагии. Аутофагия — это своего рода система утилизации клеток. Авторы делают вывод, что эти изменения — свидетельство старения. Да, в некоторых исследованиях снижение аутофагии было связано со старением. Некоторые другие авторы, однако, предполагают, что снижение аутофагии в плаценте может быть частью процесса, который фактически запускает роды, и поэтому это может быть нормальной и важной частью физиологического процесса, а не признаком того, что что-то « не так » .
Другое плацентарное изменение, процитированное в статье Маити, процитированной выше, — это апоптоз (также известный как запрограммированная гибель клеток). Апоптоз — это не просто доказательство старения. Апоптоз также происходит во время развития плода и в подростковом возрасте. Это как признак изменений, так и признак старения, и, конечно, изменения и рост очень важны в это время; весь смысл беременности в том, что малыш растет и меняется
«Роль апоптоза в нормальной физиологии так же важна, как и роль его аналога, митоза.Он демонстрирует комплементарную, но противоположную роль митоза и пролиферации клеток в регуляции различных популяций клеток. Подсчитано, что для поддержания гомеостаза в организме взрослого человека ежедневно вырабатывается около 10 миллиардов клеток только для того, чтобы уравновесить количество умирающих от апоптоза ( Renehan et al., 2001, ). И это число может значительно увеличиться, если апоптоз усиливается во время нормального развития и старения или во время болезни ».
А при беременности
«Апоптоз трофобластов является физиологическим явлением при нормальной беременности, увеличивается с увеличением срока гестации и чаще встречается при послеродовых беременностях, и поэтому считается нормальным процессом в развитии и старении плаценты.”
Снова и снова мы видим, что процессы, которые некоторые считают свидетельством старения, также можно интерпретировать как признаки нормального роста и изменений, которые являются самой функцией беременности .
Синцитиальные узлы (SNA, скопление ядер клеток (центр клеток) внутри клеток плаценты) — еще одно изменение, которое упоминается как доказательство старения:
”SNA могут формироваться для структурного усиления плаценты и минимизировать повреждение от сдвиговых напряжений или других механических источников, уменьшать долю ядер в высокоактивных васкулосинцитиальных мембранах или быть результатом обновления клеток в плаценте без триггера апоптоза или процесса выделения.В конечном счете, лучшее понимание процессов, ведущих к формированию СНС, позволит лучше понять их значение для осложнений беременности ».
Итак, то, что мы наблюдаем, может быть скорее адаптацией, чем признаком старения.
Длина теломер:
«Теломеры, ДНК-белковые структуры, расположенные на концах хромосом, были предложены как биомаркеры старения. В этом обзоре оцениваются человеческие доказательства того, что длина теломер является биомаркером старения. Хотя длина теломер участвует в старении клеток, доказательства того, что длина теломер является биомаркером старения у людей, сомнительны . Требуются дополнительные исследования, изучающие взаимосвязь между длиной теломер и смертностью, а также меры, которые снижаются с «нормальным» старением в выборках сообщества. Эти исследования выиграют от продольных измерений как длины теломер, так и параметров, связанных со старением ».
В этой статье под названием «Вопрос о причинном участии теломер в старении» авторы заявляют:
«Множественные исследования показали, что длина теломер предопределяет смертность и что теломеры укорачиваются с возрастом. Хотя эти ассоциации редко признаются, они не диктуют причинно-следственные связи . Кроме того, гипотеза причинности предполагает, что существует критическая длина теломер, при которой индуцируется старение. Это позволяет предположить, что разница в длине теломер уменьшается с возрастом. Напротив, используя метаанализ человеческих данных, я не обнаружил такого снижения. Таким образом, предположение о причинном участии теломер в старении на основе современных знаний является спекулятивным и может препятствовать научному прогрессу.”
Что меня особенно интересует, так это то, что авторы этой статьи также предполагают, что эти клеточные изменения могут быть частью того, что запускает роды:
”Старение плаценты поднимает несколько важных вопросов, которые необходимо решить экспериментально. Хотя для образования синцитиотрофобластов, по-видимому, требуется индуцированное слиянием старение, вполне вероятно, что старение как тканей плода, так и децидуальной оболочки матери играет, по крайней мере, роль в определении времени начала родов »
Так что, если то, что видно в плаценте и интерпретируется как признак старения, на самом деле является нормальными, здоровыми изменениями, которые являются признаком здорового роста и развития и могут также сыграть роль в начале родов?
Еще один «более старый» признак старения плаценты — кальцификаты.Я сам был виноват в том, что верил людям, которые говорили мне, что это признак старения, и хорошо, что ребенок родился, потому что плацента была «старой». Недавно я наткнулся на этот блог (в котором были опубликованы ссылки, подтверждающие все его утверждения):
“ Таким образом, хотя кальцификация плаценты в срок — около 39-42 недель является частью нормального внешнего вида доношенной плаценты и не имеет клинического значения для здоровой беременности, появление значительной кальцификации на ранних сроках беременности связано с с риском как для матери, так и для ребенка.Так же, как нас беспокоит очень молодой человек с морщинами — это может быть признаком чего-то значительного (…) Итак, по сути, когда мать здорова и доношена, кальциноз и инфаркты являются нормальными чертами здорового человека. плацента — как у здоровой матери есть морщинки и несколько седых волосков.
Еще один миф, вылетевший из воды.
В заключение, хотя есть доказательства клеточных изменений в плаценте на протяжении всей беременности, до сих пор нет убедительных доказательств того, что это действительно старение, а не адаптация, или что эти изменения действительно ответственны за крошечные рост числа мертворожденных, если беременность продолжается более 42 недель.
Концепция стареющей плаценты до сих пор остается только теорией. К сожалению, большинство публикаций, цитируемых в этом посте, не признают этого и принимают эту теорию как доказанную.
Что меня беспокоит еще больше, так это то, что обычно не проводится никаких консультаций с мнением женщин о процессе индукции, и эти публикации лягут в основу новых руководств NICE, а затем руководств местных больниц, и, следовательно, все больше и больше женщин будут побуждены напрасно, и иметь негативный или травмирующий опыт.
Это поддерживает текущую тенденцию к индукции женщин еще раньше, в 39 недель вместо нынешних 41–42 недель.
Рождение, основанное на доказательствах, явилось прекрасным обзором литературы по этой теме.
Я надеюсь, что чтение этого блога поможет женщинам и их сторонникам принимать осознанные решения.
Я также хотел бы призвать ученых и политиков сохранять любопытство в отношении более широкой картины и больше взаимодействовать с беременными женщинами и их взглядами на процесс индукции.
Я благодарен Мэдди МакМахон за редактирование этого блога
Если это находит отклик у вас и вы хотели бы поработать со мной, отправляйтесь сюда, если вы беременная или молодая мама, или сюда, если вы роженица.
Если вы нашли этот блог полезным и хотели бы поддержать мою работу и помочь мне продолжать предоставлять ценную бесплатную информацию роженицам, беременным и новорожденным семьям, вы можете сделать пожертвование на мою учетную запись PayPal paypal.me/SophieMessager.
Также не стесняйтесь подписаться на мой список рассылки, чтобы получать мои информационные бюллетени, используя форму подписки внизу этой страницы
Миф о старении плаценты
В 2018 году была одна тема, по которой мы получили больше комментариев, писем и запросов, чем все остальное вместе взятое: индукция родов.Да, наверное, отчасти потому, что я сам об этом писал. Но я писал и о множестве других тем, и индукция родов по-прежнему остается самой обсуждаемой.
Когда мы вкратце проанализировали характер и содержание полученных нами комментариев, многие выразили обеспокоенность по поводу роста числа вводных. Мы слышали от многих женщин, которым сказали, что им «нужна» индукция или что их ребенок «находится в опасности», но при этом не получили убедительных доказательств в поддержку этого утверждения.
Одна проблема, о которой мы слышали больше, чем когда-либо, была от женщин, которым сказали, что их ребенок находится в опасности, потому что их плацента «недостаточна» или «стареет».Я немного написал об этом, отметив, что, «Проблема в том, что концепция плацентарной недостаточности может быть описана как довольно« скользкая », и нет никаких доказательств того, что существует корреляция между плацентарной недостаточностью и продолжительностью плацентарной недостаточности. беременность. Как любит говорить мой друг-акушер, если плацента женщины плохо работает на 23 неделе, то вряд ли она будет хорошо работать к 39 неделе. Но если он работает хорошо на 40 или 41 неделе, тогда нет веских оснований полагать, что его функция внезапно ухудшится в течение следующих нескольких дней.” (Wickham 2018)
Но нам действительно нужно было более аргументированное обсуждение теории старения плаценты, поэтому я был очень рад увидеть публикацию этой статьи — Миф о старении плаценты — доктора Софи Мессагер, преподавателя доулы и родовспоможения, которая также имеет докторскую степень по физиологии репродукции и двадцатилетний исследовательский опыт. Статья длинная и подробная, поэтому, как она рекомендует сама, вы можете приготовить себе чашку чая, прежде чем сесть за нее!
Есть несколько вещей, которые я особенно ценю в статье доктора Мессагера.Во-первых, она предлагает важную дискуссию о том, как теории, подобные этой, иногда представляются определенными группами как общепринятый факт, когда еще много споров, неопределенности и разногласий. Научный опыт д-ра Мессагер позволяет ей утверждать, что даже (или, возможно, особенно) на самом высоком уровне научного прогресса и дискуссий эксперты часто не соглашаются друг с другом. Я могу подтвердить это и на собственном опыте; Я считаю, что мне повезло, что в моем кругу общения много других академиков и ученых, и я сидел и участвовал в горячих (хотя, как правило, профессиональных, уважительных, дружеских и иногда юмористических) дебатах по темам от археологии до транспортной географии (тема, которую часто обсуждают. в нашем доме, так что будьте осторожны, если приедете на ужин).Я рано заметил в своей жизни, что, как правило, чем умнее человек, тем больше он склонен слушать других и тем меньше вероятность того, что он будет догматичен относительно того, что «правильно» или «неправильно».
Это связано с еще одним очень важным моментом: не всегда есть правильное или неправильное, и наши знания постоянно растут и меняются. Многие вещи, которым я научилась, будучи студенткой-акушеркой около двадцати пяти лет назад, теперь изменились. Например, иллюстрации анатомии груди, которые были доступны, когда я узнал об анатомии грудного вскармливания, больше не считаются точными.Но будет ли пересмотренная картина, которую мы имеем сегодня, по-прежнему считать «истинной» и / или актуальной в следующие двадцать пять лет? Ну кто знает! Знания не являются фиксированными или достоверными, и утверждает, что к ним следует относиться с осторожностью; они часто много говорят о мышлении человека, делающего заявление.
Если вы акушерка или работник родовспоможения и хотите укрепить свою уверенность в доказательствах, касающихся переношенной беременности и индукции родов, я провожу популярный онлайн-курс по этой теме один раз в год — нажмите здесь, чтобы найти узнайте больше или зарегистрируйтесь.
Но часть сообщения в блоге доктора Мессагер, которая мне показалась наиболее поучительной, заключалась в том, когда она, опираясь на свой собственный научный опыт в области физиологии репродукции, рассматривала каждое из изменений, которые приводятся в качестве доказательства старения плаценты и показывали как их также можно интерпретировать как просто признаки изменений, связанных с ростом и развитием, а именно то, что должны делать наши плаценты и младенцы. Это важный элемент дискуссии, который требует дальнейшего обсуждения.Как я отмечал в книге «Побуждение к родам: принятие обоснованных решений», , «наша современная культура не очень терпима к концепции старения в целом, особенно у женщин, поэтому неудивительно, что мы так легко принимаем идею о том, что стареющая плацента нежелательна. и проблематично ». (Уикхэм 2018)
На протяжении своей карьеры я видел много примеров теорий, которые были предложены, часто кем-то, кто хотел сделать себе имя (и, возможно, также дать его части анатомии женщины, процедуре или продаваемому инструменту), и которые были позже было показано, что они ложны и потенциально вредны.И да, я также видел, как теории со временем становятся более достоверными и ценными. Возможно, ключ кроется в умении различать знания, доказательства и мудрость.
Еще раз процитирую доктора Мессагера: «Концепция стареющей плаценты все еще остается только теорией. К сожалению, большинство публикаций, цитируемых в этом посте, не признают этого и принимают эту теорию как доказанную ». Я рекомендую прочитать сообщение в блоге полностью, если вы хотите углубиться в эту область.
Если вас интересуют исследования, связанные с рождением, нажмите здесь, чтобы перейти к списку адресов электронной почты Сары и получать наш бесплатный ежемесячный бюллетень с обновлениями об исследованиях и мышлении, связанных с родами. Мы также публикуем сообщения в нашем блоге каждый месяц!
Нравится:
Нравится Загрузка …
СвязанныеКакие нарушения могут повлиять на плаценту во время беременности?
Плацента и ее здоровье имеют жизненно важное значение для здоровья женщины во время беременности и развития плода.Этот орган обеспечивает кислород, питательные вещества и фильтрует отходы плода во время беременности.
Он также играет важную роль в производстве гормонов и защищает плод от бактерий и инфекций.
Плацента, обогащенная кровью, соединяется со стенкой матки и соединяется с ребенком через пуповину.
Чаще всего плацента прикрепляется к верхней или боковой стенке матки. Однако иногда он может расти или прикрепляться к матке, что может вызвать проблемы со здоровьем.
Поделиться на PinterestПлацента играет жизненно важную роль для развивающегося плода во время беременности.Многие факторы влияют на здоровье плаценты, в том числе:
- этническая принадлежность
- история курения сигарет
- высокое кровяное давление
- многоплодная беременность
- нарушения свертываемости крови у матери
- история хирургических вмешательств на матке, таких как кесарево сечение
- история проблем с плацентой
- злоупотребление психоактивными веществами у матери, например, употребление кокаина
- травма живота, например, в результате падения или тупой травмы
- возраст матери, поскольку женщины старше 40 лет имеют более высокий риск развития проблем с плацентой
- преждевременный разрыв плодных оболочек, потому что риск проблем с плацентой увеличивается, если амниотический мешок разрывается слишком рано
Существует множество осложнений, которые могут повлиять на плаценту.Ниже описаны наиболее распространенные расстройства.
Предлежание плаценты — это состояние, при котором плацента прикрепляется к стенке матки очень низко. При этом плацента частично или полностью покрывает шейку матки.
Этим заболеванием страдает 1 из 200 женщин в третьем триместре. Однако состояние может исчезнуть по мере прогрессирования беременности.
Факторы риска
Предлежание плаценты чаще встречается у женщин, которые:
- старше
- курят
- перенесли кесарево сечение или другие операции на матке
- вынашивают многоплодную беременность
Есть типы
Есть три типа предлежания плаценты:
- Маргинальное: плацента доходит до края шейки матки
- Полное: предлежание плаценты полностью покрывает шейку матки
- Частично: плацента частично покрывает шейку матки
Предлежание плаценты может вызывать вагинальные кровотечение как до, так и во время родов.Это кровотечение может быть серьезным и может потребовать лечения.
Осложнения
Помимо кровотечения, предлежание плаценты может вызвать следующие осложнения во время беременности:
- разрыв плаценты
- повышенный риск инфицирования плода
- схватки
- преждевременные роды
Чаще всего необходимо кесарево сечение для безопасных родов.
Отслойка плаценты происходит, когда плацента отделяется от матки во время беременности.Отслойка может быть как частичной, так и полной.
Заболевание чаще всего возникает в третьем триместре. Это наиболее распространенное плацентарное заболевание, которое встречается примерно в 1 из 100 беременностей.
Отслойка плаценты — основная причина смерти плода и новорожденного.
Он также вызывает высокие показатели преждевременных родов и задержки роста плода.
Факторы риска
Риск отслойки плаценты может быть увеличен:
- травмой живота
- преждевременным разрывом мембраны
- курением матерью или отцом
- употреблением кокаина или алкоголя
- предшествующим плацентарным анамнезом отслойка
- с предлежанием плаценты
- дефект матки
- высокое кровяное давление у матери или высокое кровяное давление, вызванное беременностью
- окантовка плаценты
- предыдущее кесарево сечение или прерывание
- вынашивание более одного плода
- аномальное сердцебиение плода
Симптомы и диагностика
Будущие матери с отслойкой плаценты могут испытывать вагинальное кровотечение, боль в матке или животе, постоянные схватки и нарушения сердечного ритма плода.
Диагноз отслойки плаценты будет основан на симптомах и лечиться в зависимости от их степени тяжести.
Осложнения
Из-за той роли, которую плацента играет в доставке кислорода и питательных веществ, отслойка плаценты может вызвать лишение этих жизненно важных питательных веществ.
Эта депривация может привести к аномальному развитию плода, преждевременным родам, задержке роста плода и мертворождению.
Поделиться на PinterestПлацентарная недостаточность связана с преэклампсией, причиной высокого кровяного давления во время беременности.Как обсуждалось ранее, плацента играет жизненно важную роль в развитии плода, обеспечивая растущего ребенка питательными веществами и кислородом и фильтруя его продукты жизнедеятельности.
Однако иногда плацента может не функционировать должным образом. Когда это происходит, он может не обеспечивать адекватное количество питания, вызывая плацентарную недостаточность. Это происходит в 1 из 300 беременностей.
Эта аномалия плаценты часто приводит к задержке роста плода и низкой массе тела при рождении у младенцев.
Женщины с плацентарной недостаточностью могут заметить меньшее шевеление плода и меньший размер матки, чем раньше.
Факторы риска
Это чаще встречается у матерей, которые:
- болеют преэклапсией
- болеют диабетом
- курят или употребляют рекреационные препараты
- имеют проблемы со свертыванием крови или принимают препараты для разжижения крови
могут быть последствия как для матери, так и для плода, связанные с плацентарной недостаточностью. Риски для матери возрастают при наличии диабета и высокого кровяного давления.
Симптомы
Симптомы плацентарной недостаточности включают:
- отслойка плаценты (см. Выше)
- преждевременные роды
- преэклампсия.
Преэклампсия характеризуется высоким кровяным давлением и наличием белка в моче. Симптомы преэклампсии включают чрезмерное увеличение веса, отеки, головные боли и высокое кровяное давление.
Осложнения
Риски для плода и младенца при наличии плацентарной недостаточности включают:
- кислородное голодание при рождении, которое может вызвать такие состояния, как церебральный паралич
- нарушение обучаемости
- гипотермия или низкая температура тела
- гипогликемия, или низкий уровень сахара в крови
- полицитемия или чрезмерный уровень эритроцитов
- преждевременные роды
- необходимость кесарева сечения
- мертворождение или смерть
Наличие плацентарной недостаточности на ранних сроках беременности усугубляет проблемы, с которыми сталкиваются детка.
Нет лекарства от плацентарной недостаточности, но крайне важно получить рекомендованное последующее наблюдение и дородовой уход.
Медицинские работники могут регулярно оценивать вашу беременность, рекомендуя:
- более частые осмотры в офисе
- записи о подсчете ударов
- обучение самоконтролю симптомов преэклампсии
- постельный режим
- инъекции стероидов до 32 недель при преждевременных родах риск
- осмотр у специалиста
В тяжелых случаях будущим мамам может потребоваться пребывание в стационаре.
Инфаркт плаценты — это участки мертвой ткани внутри плаценты, обычно вызванные осложнениями со стороны кровеносных сосудов.
Эта аномалия плаценты снижает приток крови к пораженным участкам. Иногда это может вызвать задержку роста плода или смерть. Инфаркты плаценты чаще возникают у женщин с высоким кровяным давлением.
Поделиться на Pinterest Кесарево сечение может увеличить риск приросшей плаценты в будущем.Приросшая плацента — серьезное заболевание, которое встречается у 1 из 2500 беременностей.
Плацента и ее кровеносные сосуды прикрепляются и врастают глубоко в стенку матки.
Существует три формы:
- Приросшая плацента: Плацента прикрепляется к мышце стенки матки
- Приращение плаценты: Плацента прикрепляется через мышцу стенки матки
- Плацента перкрета: Плацента растет через всю стенку матки и прикрепляется к другим окружающим органам.
Факторы риска развития приросшей плаценты в основном неизвестны.Считается, что они включают в себя предлежание плаценты и предыдущее кесарево сечение.
Осложнения этого состояния могут включать вагинальное кровотечение в третьем триместре, тяжелое послеродовое кровотечение, кесарево сечение и последующую гистерэктомию.
Поговорите со своим врачом, чтобы обсудить ваш личный риск развития аномалий плаценты и дать рекомендации по профилактике и лечению.
Маленький для гестационного возраста | Детская больница Филадельфии
Маленький для гестационного возраста — это термин, используемый для описания ребенка, размер которого меньше обычного для данного количества недель беременности.Дети с SGA обычно имеют массу тела при рождении ниже 10-го процентиля для детей того же гестационного возраста. Это означает, что они меньше, чем многие другие дети того же гестационного возраста.
Младенцы SGA могут казаться физически и неврологически зрелыми, но меньше других детей того же гестационного возраста. Младенцы SGA могут быть пропорционально маленькими (одинаково маленькими по всему телу) или могут иметь нормальную длину и размер, но иметь меньший вес и массу тела. Дети с SGA могут быть недоношенными (родившимися до 37 недель беременности), доношенными (от 37 до 41 недели) или доношенными (после 42 недель беременности).
Хотя некоторые дети маленькие из-за генетики (их родители маленькие), большинство детей с SGA маленькие из-за проблем роста плода, возникающих во время беременности. Многие дети с SGA имеют состояние, называемое задержкой внутриутробного развития (IUGR). ЗВУР возникает, когда плод не получает необходимых питательных веществ и кислорода, необходимых для правильного роста и развития органов и тканей. ЗВУР может начаться на любом сроке беременности. Раннее начало ЗВУР часто связано с хромосомными аномалиями, материнскими заболеваниями или серьезными проблемами с плацентой.Задержка роста (после 32 недель) обычно связана с другими проблемами.
Некоторые факторы, которые могут способствовать SGA и / или IUGR, включают следующее:
Когда плод не получает достаточного количества кислорода или питательных веществ во время беременности, общий рост тела и органов ограничен, а клетки тканей и органов могут не расти в таких размерах или в таком количестве. Некоторые из состояний, вызывающих SGA и IUGR, ограничивают кровоток через плаценту. Это может привести к тому, что плод будет получать меньше кислорода, чем обычно, что увеличивает риски для ребенка во время беременности, родов и после них.
Младенцы с SGA и / или IUGR могут иметь проблемы при рождении, включая следующие:
Пониженный уровень кислорода
Низкие баллы по шкале Апгар (оценка, помогающая выявлять детей с трудностями адаптации после родов)
Аспирация мекония (вдыхание первых дефекаций в утробе матери), которая может вызвать затруднение дыхания
Гипогликемия (низкий уровень сахара в крови)
Нарушение поддержания нормальной температуры тела
Полицитемия (слишком много красных кровяных телец)
Ребенок с SGA часто выявляется еще до рождения.Во время беременности размер малыша можно оценить по-разному. Высота глазного дна (верхняя часть матки матери) может быть измерена от лобковой кости. Это измерение в сантиметрах обычно соответствует количеству недель беременности после 20-й недели. Если для количества недель измерения низкие, ребенок может быть меньше, чем ожидалось.
Хотя многие дети с SGA имеют низкий вес при рождении, не все они являются недоношенными и могут не испытывать проблем, связанных с недоношенными детьми.Другие дети с SGA, особенно с IUGR, кажутся худыми, бледными и с дряблой сухой кожей. Пуповина часто бывает тонкой и тусклой, а не блестящей и толстой.
Другие диагностические процедуры могут включать следующее:
УЗИ. Ультразвук (тест с использованием звуковых волн для создания изображения внутренних структур) — более точный метод оценки размера плода. Можно измерить голову и живот плода и сравнить их с диаграммой роста для оценки веса плода.Окружность живота плода является полезным индикатором питания плода.
Доплеровский поток. Еще один способ интерпретировать и диагностировать ЗВУР во время беременности — это допплеровский кровоток, который использует звуковые волны для измерения кровотока. Звук движущейся крови создает волны, отражающие скорость и количество крови, движущейся по кровеносному сосуду. Кровоток через кровеносные сосуды как в головном мозге плода, так и в пуповине можно проверить с помощью допплеровских исследований кровотока.
Увеличение веса матери. Набор веса матери также может указывать на рост ребенка. Небольшая прибавка в весе у матери во время беременности может соответствовать рождению маленького ребенка
Оценка беременности. Младенцы взвешиваются в течение первых нескольких часов после рождения. Вес сравнивается с гестационным возрастом ребенка и записывается в медицинскую карту. Вес при рождении необходимо сравнить с сроком беременности. Некоторые врачи используют формулу для расчета массы тела ребенка для диагностики SGA.
Специфическое лечение SGA определит врач вашего ребенка на основании:
Гестационный возраст, общее состояние здоровья и история болезни вашего ребенка
Степень условия
Толерантность вашего ребенка к определенным лекарствам, процедурам или методам лечения
Ожидания по ходу состояния
Ваше мнение или предпочтение
Младенцы с SGA могут быть физически более зрелыми, чем указывает их небольшой размер.Но они могут быть слабыми и хуже переносить обильные кормления или оставаться в тепле. Лечение ребенка SGA может включать:
Кровати или инкубаторы с регулируемой температурой
Кормление через зонд (если ребенок не сосет сильно)
Проверка на гипогликемию (низкий уровень сахара в крови) с помощью анализов крови
Контроль уровня кислорода
Младенцы с SGA и недоношенные дети могут иметь дополнительные потребности, включая кислород и механическую помощь для дыхания.
Пренатальный уход важен при всех беременностях, особенно для выявления проблем, связанных с развитием плода. Отказ от курения и употребление таких веществ, как наркотики и алкоголь, необходимы для здоровой беременности и могут снизить риск синдрома внезапной детской смерти (СВДС) и других младенческих смертей, связанных со сном. Также может помочь здоровое питание во время беременности.
.